Процесс - переход - электрон
Cтраница 3
Если законы движения электронов в таких аморфных материалах и отличаются существенно от движения их в кристаллической среде, то существование дискретного энергетического спектра и, в частности, запретных зон, процессы перехода электронов под действием теплового движения с одного квантового уровня на другой, процессы рекомбинации, диффузии и статистического равновесия столь же свойственны аморфным телам, как и кристаллам. Решающим для тех и других являются межатомные связи и расстояния, а также квантовые состояния электронов, совместимые с этими расстояниями. [31]
На основании этого факта, учитывая работы М. И. Темкина [ У ], в которых показана определенная связь между кинетическими адсорбционными характеристиками различных мест неоднородной поверхности, приводящая к кинетическим уравнениям с дробными показателями степени для некоторых гетерогенных каталитических процессов, Чжоу Шао-минь пришел к выводу, что в электрохимической реакции участвуют толь-ко молекулы спирта, адсорбированные на поверхности анода, и лимитирующей стадией в процессе окисления, соответствующем восходящим ветвям поляризационных кривых, является процесс перехода электрона от адсорбированной частицы к аноду. [32]
Рассмотрим на основании приведенных общих соображений [2, 3] наиболее простую и хорошо изученную реакцию, протекающую на поверхности металла - реакцию выделения водорода. Процесс перехода электрона из металла в раствор по принципу Франка-Кондона возможен лишь тогда, когда энергии электрона в металле ( начальное состояние) и в атоме водорода ( конечное состояние) одинаковы. Ни для одного из металлов это равенство в общем случае не выполняется. Так как энергия активации реакции выделения водорода положительна, то для выравнивания уровней необходимо, чтобы энергия электронов в атоме водорода понизилась до уровня Ферми, или энергия электрона в металле поднялась до его уровня в атоме водорода. [33]
Свободные электроны движутся в междуатомном пространстве беспорядочно и в силу этого временами опять попадают на орбиты к своим или к другим атомам, также временно лишившимся электронов. Процесс перехода электронов на орбиты или в свободное состояние продолжается непрерывно, однако в любой момент времени в теле имеется определенное количество свободных электронов. Это количество определяется структурой атомов, поэтому различно в разных металлах и сплавах. В чистых металлах, особенно в серебре, свободных электронов очень много, в сплавах их значительно меньше. [34]
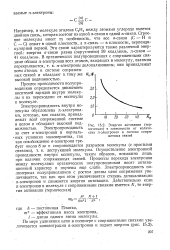 |
Энергия активации ( термическая в зависимости от количества я-электронов в системе сопряженных связей. [35] |
Осуществление электронной проводимости внутри молекулы, таким образом, возможно лишь при наличии сопряженных связей. Процессы перехода электронов между молекулами органических полупроводников носят актива-ционный характер и изучены еще слабо. Электропроводность полимерных полупроводников с ростом длины цепи сопряжения увеличивается, так как при этом увеличивается степень делокализации я-электронов и снижается энергия активации. [36]
Изменение работы выхода, наблюдаемое при адсорбции газа на поверхности металла, обусловлено электронным взаимодействием между металлом и адсорбатом. В большинстве случаев хемосорбция сопровождается процессом перехода электронов, природа которого зависит от электронного строения и поверхностных свойств металла. Поэтому желательно прежде всего pat - смотреть в общих чертах процесс адсорбции и образование химических связей с поверхностью металла. [37]
Локальные уровни в запрещенной зоне полупроводника могут быть эффективными центрами рекомбинации, если они расположены вдали от дна зоны проводимости и потолка валентной зоны, в противном случае они играют роль уровней прилипания, так как захваченный ими носитель через некоторое время выбрасывается в свою зону. Центры рекомбинации часто называют ловушками, а процесс перехода электрона из зоны проводимости на свободный уровень рекомбинации - захватом электрона ловушкой. Аналогично этому переход электрона с ловушки на свободный уровень в валентной зоне и освобождение уровня ловушки называют захватом дырки ловушкой. [38]
В исследованных ферритах содержались ионы двухвалентного железа, присутствие которых и обусловливает релаксацию. Низкое значение энергии активации и позволяет рассматривать это последействие как процесс перехода электронов между ионами Fe2 и Ре3, который приводит к перераспределению этих ионов по октаэдр ическим положениям решетки шпинели в зависимости от действия магнитострикционных сил ( см. гл. [39]
Остается еще разобрать полярографическое осаждение нерастворимых в ртути металлов. При этом необходимо рассмотреть довольно редкий случай обратимого выделения металла на электроде без торможения, процессов перехода электрона и образования кристаллических зародышей. На поверхности ртути появляется пленка выделяющегося металла, который не может диффундировать внутрь капли вследствие нерастворимости. [40]
Значительно больший интерес представляет исследование зависимости изменения разности потенциалов в гельмгольцевском двойном слое от конфигурации поверхностных состояний и объемных свойств полупроводника. Особый интерес представляет разность потенциалов S 6, возникающая в результате разделения заряженных частиц в гельмгольцевском двойном слое, в котором осуществляется процесс перехода электрона. [41]
Если металл привести в контакт с полупроводником, то электроны устремятся из полупроводника в металл. Процесс перехода электронов продолжается до тех пор, пока не совпадут уровни Ферми металла и полупроводника. [42]
Таким образом второй канал реакции наиболее вероятен. Поэтому здесь его и рассмотрим, предварительно предположив, что число протонов-акцепторов в растворе существенно превосходит число вылетающих с поверхности металла электронов. В этом случае процесс перехода электронов из металла в раствор будет подобен процессу вылета термоэлектронов из металла в вакуум, где число вакантных мест бесконечно велико. Чтобы подчеркнуть эту аналогию, мы сначала не будем конкретизировать физический смысл потенциального барьера, который в термоэлектронной эмиссии представляет работу выхода электрона W из металла в окружающую среду, подразумевая под ней просто разность энергий электрона в среде и в металле. [43]
В действительности же этот процесс еще сложнее, так как рассмотренные ступени в свою очередь также состоят из многих частичных процессов. Так, например, процесс перехода электрона к катиону сам состоит из многих стадий. Затем электрон присоединяется к катиону, и, хотя при этом может освобождаться энергия, катион должен быть предварительно дегидратирован, что снова требует затраты энергии. Образовавшийся атом адсорбируется на поверхности электрода, при этом энергия освобождается. Кроме того, атом мигрирует по внешней поверхности электрода, что в свою очередь требует ослабления адсорбционных связей. Данные стадии процесса можно было бы еще более детализировать, но это увело бы нас слишком далеко. [44]
Каталитические процессы имеют большое значение в аналитической химии, потому что их легко можно осуществить в виде избирательных, а иногда и специфичных реакций. Особенно это относится к гомогенным каталитическим реакциям в жидкой фазе. Так, простые ионы многовалентных металлов могут ускорять процессы перехода электронов. Каталитическими свойствами часто обладают также протолиты. Гетерогенный катализ, в котором катализатор составляет отдельную фазу, имеет в химическом анализе второстепенное значение. [45]
Страницы: 1 2 3 4