Процесс - получение - азотная кислота
Cтраница 3
Понижение температуры способствует также увеличению скорости реакций, в особенности реакции окисления окиси азота, скорость которой определяет общую продолжительность процесса получения азотной кислоты. Так, снижение температуры поглощения с 40 до 20 С позволяет повысить производительность системы, в 1 5 раза, а понижение температуры с 40 до 0 С приводит к увеличению производительности в 2 раза. Понижение температуры процесса поглощения позволяет получать более концентрированную азотную кислоту. [31]
 |
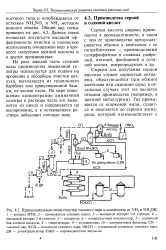
Принципиальная схема очистки сокового пара и конденсата от NH3 и NH4OH. [32] |
Принцип работы установки понятен из рис. 11.2. Данная схема позволяет достигнуть высокой эффективности очистки и полностью использовать очищенную воду в процессе получения азотной кислоты и в других производствах. [33]
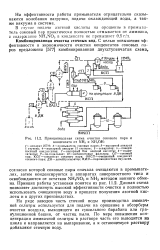
Общий вид схемы приведен на рис. 4.2. Данная схема позволяет достигнуть высокой эффективности очистки и полностью использовать очищенную воду в процессе получения азотной кислоты и в других производствах. [35]
Для осуществления контроля и регулирования технологического процесса и производстве азотной кислоты применяется пневматическая система, t которой предусмотрена возможность перехода на дистанционное управление Автоматическое регулирование процесса получения азотной кислоты прсжд ( нсето основано на регулировании соотношения расхода аммиака и воздуха давления и температуры на катализэторных сетках, давления и уровня водь н паровом ко Гле, концентрации продукционной кислоты. Для стабилиэацш состава аммиачпо-воздушнои г. мсси установлены регуляторы соотношенш количеств аммиака и воздуха; температур аммиачпо-воэдушной смеси, подогретого воздуха, каталиэаторлых сеток, питрозних газов после котла утили - Затора, окислителя, на входе в абсорбционную колонну и на выходе из нее Эти тюкаэапия, как иравило, фиксируются самопишущими приборами непрерывно записываются. [36]
Концентрации озона, превышающие предельно допустимые нормы, могут быть не только в помещениях, где находится установка его получения, но и в лабораториях, занимающихся изучением процессов получения азотной кислоты, перекиси водорода, электролизом воды, а также в лабораториях спектрального, рентгеновского, электронографического анализа. Он служит также исходным веществом для получения неорганических и органических озонидов. [37]
 |
Микропоглотительный сосуд. [38] |
Одним из источников отравления рабочих при взрывных работах в подземных выработках является выделение в шахтный воздух окислов азота и других продуктов взрыва. Двуокись азота в опасных концентрациях встречается также в воздухе промышленных предприятий, преимущественно при процессах получения азотной кислоты, при нитровании, в сернокислотном производстве, при электро - и ацетиленовой сварке. [39]
Из сплавов платины с родием изготавливают катализаторные сетки, на которых при температуре 800 - 900 С происходит окисление аммиака в окислы азота - главная стадия процесса получения азотной кислоты. Присадка 5 - 10 % родия повышает намного прочность сетки, и потери платины в процессе производства уменьшаются в полтора-два раза. Более того, эта присадка увеличивает каталитическую активность. Производство азотной кислоты на платинородиевых сетках сейчас исчисляется десятками миллионов тонн в год и требует ежегодно несколько сот килограммов родия. [40]
Из сплава платины с родием изготавливают ка-тализаторпыс сетки, па которых при температуре 800 - 900 С происходит окисление аммиака в окислы азота - главная стадия процесса получения азотной кислоты. Присадка 5 - 10 % родия намного повышает прочность сетки, и потери платины в процессе производства уменьшаются в полтора - два раза. Более того, эта присадка увеличивает каталитическую активность. Производство азотной кислоты на платинородиевых сетках сейчас исчисляется десятками миллионов тонн в год и требует ежегодно нескольких сот килограммов родия. [41]
Рассмотрение равновесия и кинетики реакций приводит к заключению о необходимости осуществлять переработку н и т розных газов в азотную кислоту при пониженных температурах. Единственной реакцией, на которую понижение температуры влияет отрицательно, является эндотермическая реакция разложения азотистой кислоты, которая, однако, и при пониженных температурах не контролирует всего процесса получения азотной кислоты. Все остальные реакции, протекающие при переработке окиси азота в азотную кислоту, являются экзотермическими, и равновесие их смещается в благоприятную для образования азотной кислоты сторону при понижении температуры. Понижение температуры благоприятно сказывается также и на увеличении скорости реакций, в особенности реакции окисления окиси азота, скорость которой решает вопрос об общей продолжительности процесса получения азотной кислоты. Так, понижение температуры процесса поглощения с 40 до 20 позволяет повысить производительность системы в 1 5 раза, а понижение температуры с 40 до 0 -в 2 раза. Понижение температуры процесса поглощения позволяет получать и более концентрированную азотную кислоту. [42]
Для подавляющего большинства реакций характерно увеличение скорости с повышением температуры, но реакция окисления NO в NO2 не подчиняется этому общему правилу и скорость ее уменьшается с повышением температуры. Таких реакций немного и их называют аномальными. Окисление NO в NO2 является наиболее медленной стадией процесса получения азотной кислоты. Поэтому для установок, работающих под атмосферным давлением, требуются большие по объему окислительно-абсорбционные башни. [43]
Для подавляющего большинства реакций характерно увеличение скорости с повышением температуры, но реакция окисления NO в МО2 - не подчиняется этому общему правилу и скорость ее уменьшается с повышением температуры. Таких реакций немного и их называют аномальными. Окисление NO в NO2 является наиболее медленной стадией процесса получения азотной кислоты. Поэтому для установок, работающих под атмосферным давлением, требуются большие по объему окислительно-абсорбционные башни. [44]
Рассмотрение равновесия и кинетики реакций приводит к заключению о необходимости осуществлять переработку нитрозных газов в азотную кислоту при пониженных температурах. Единственной реакцией, на которую понижение температуры влияет отрицательно, является эндотермическая реакция разложения азотистой кислоты. Однако эта реакция и при пониженных температурах не контролирует всего процесса получения азотной кислоты. Все остальные реакции, протекающие при переработке окиси азота в азотную кислоту, являются экзотермическими, и при понижении температуры равновесие их смещается в сторону, благоприятную для образования азотной кислоты. [45]
Страницы: 1 2 3 4