Процесс - электрохимический синтез
Cтраница 3
Как следует из наших работ [14,60], важную роль в процессе электрохимического синтеза играет низкая температура, которая повышает устойчивость промежуточных, термодинамически неустойчивых при обычных температурах соединений, приводя к увеличению их поверхностной концентрации и возрастанию вероятности того, что эти соединения или радикалы будут взаимодействовать друг с другом или с другими разряжающимися частицами электролита, образуя новые соединения. [31]
Кроме определяющей роли поверхности электрода в стабилизации первично генерированных, активных в процессе электрохимического синтеза частид, очень важдую роль играет температура электрода. В изложенном материале процессу низкотемпературного синтеза отведено особенное внимание и показано, что снижение температуры действующего электрода приводит к получению принципиально новых, как правило, богатых энергией химических соединений, в частности высших кислородных соединений. Главной причиной является здесь стабилизация при низкой температуре первично образовавшихся в результате акта разряда и адсорбированных на электроде активных частиц. Так, разряд иона ClOj при обычных температурах приводит к выделению кислорода или ( при высоких концентрациях ClOj -) к образованию С1О2 ввиду распада СЮ - радикала. [32]
Пористость графита, приводящая к быстрому износу анодов, препятствует применению его в процессах электрохимического синтеза. [33]
Рассмотрим некоторые проблемы, которые в настоящее время решаются на пути повышения основных показателей процессов электрохимического синтеза. Из них наиболее важными являются: 1) повышение производительности электролизера ( интенсификация процесса электролиза), 2) снижение расхода электроэнергии, 3) уменьшение потерь вещества за счет диффузии через диафрагму. [34]
Низшие углеводороды - предельные и непредельные - могут с успехом служить исходным сырьем во многих процессах электрохимического синтеза. [35]
Исследованы условия электролитического осаждения двуокиси свинца в форме, пригодной для применения в качестве нерастворимого анода в процессах электрохимического синтеза. [36]
 |
Зависимость удельной электропроводимости растворов NaOH от концентрации при различных температурах. [37] |
Поляризация, обусловленная скоростью массопереноса исходного вещества к поверхности электрода и отвода продуктов электролиза в объем раствора, что особенно часто наблюдается в процессах электрохимического синтеза, может быть снижена путем проведения электролиза в режиме интенсивного перемешивания электролита. В последнее время особенно широкое развитие получили процессы, в которых перемешивание создается за счет интенсивной циркуляции раствора через электролизер. [38]
Наибольшее внимание было уделено разработке эффективного метода электрохимической гидродимеризации акрилонитрила в адипонитрил [14 - 18], являющийся ценным исходным полупродуктом в производстве полиамидных смол. Особенностью процессов электрохимического синтеза адипонитрила и других ди-нитрилов является проведение их в водных растворах гидротроп-ных солей, которые служат электролитами. [39]
Приведенный в статье материал показывает, что электрохимические методы начинают находить применение для синтеза различных классов органических соединений с высокой степенью чистоты. Особенный интерес представляют процессы электрохимического синтеза в крупнотоннажных производствах некоторых мономеров ( адипонитрил, гексаметилендиамин, высшие дикарбоновые кислоты) благодаря возможности использования доступных видов сырья. Вследствие этого в некоторых случаях электрохимические методы получения органических соединений оказываются экономически выгодными. Ярким примером сказанного является электрохимический метод получения адипонитрила, который в настоящее время внедряется в промышленном масштабе в ряде стран. [40]
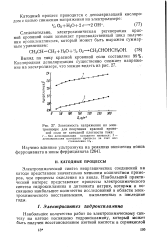 |
Зависимость напряжения на электролизере для получения красной кровяной соли от катодной плотности тока. [41] |
Электрохимический синтез неорганических соединений на катоде представлен значительно меньшим количеством примеров, чем процессы окисления на аноде. Наибольший практический интерес представляют процессы электрохимического синтеза гидроксиламина и дитионита натрия, которым и посвящено наибольшее количество исследований в области электрохимического восстановления, выполненных в последние годы. [42]
Совмещение реакций на одном и том же электроде наблюдается довольно часто. Так, при проведении процессов электрохимического синтеза на основную катодную реакцию накладывается реакция выделения водорода, а на основную анодную - выделения кислорода. [43]
Электрохимический синтез неорганических соединений на катоде представлен значительно меньшим количеством процессов, чем окисление на аноде. Наиболее интересны в практическом отношении процессы электрохимического синтеза гидроксиламина, применение электролиза для каталитической фиксации азота, получение дитионита натрия, перекиси водорода, которым и посвящено значительное количество исследований в области электрохимического восстановления, выполненных в последние годы. [44]
Несколько отличной областью применения электрохимических методов в органическом синтезе является восстановление органических соединений амальгамой натрия в аппаратах-разлагателях при производстве хлора с применением ртутных катодов. Однако в настоящей главе рассматриваются только процессы прямого электрохимического синтеза органических соединений. [45]
Страницы: 1 2 3 4