Процесс - кислотно-основное взаимодействие
Cтраница 1
Процессы кислотно-основного взаимодействия в водно-органических смесях характеризуются чрезвычайно сложной зависимостью термодинамических функций от состава растворителя, в особенности при большом содержании воды. [1]
Процессы кислотно-основного взаимодействия в смесях оснований и солей слабых кислот можно представить подобно процессам, рассмотренным для смесей кислот и солей слабых оснований. [2]
Процесс кислотно-основного взаимодействия может остановиться на любой стадии приведенной схемы. В результате взаимодействия могут образоваться как молекулы НАВ или ионизированный комплекс НВ А и раствор неэлектролита, так и ионы НВ и А и раствор электролита. [3]
Процесс кислотно-основного взаимодействия может остановиться на любой стадии приведенной схемы. В результате взаимодействия могут образоваться как молекулы НАВ или ионизированный комплекс НВ А - и раствор неэлектролита, так и ионы НВ и А и раствор электролита. [4]
Многие процессы кислотно-основного взаимодействия протекают очень быстро, но благодаря современной технике физико-химического эксперимента представилась возможность исследовать их. [5]
Скорость процессов кислотно-основного взаимодействия можно регулировать, изменяя реакционную активность наполнителя за счет уплотнения и укрупнения его частиц, а также применяя дисперсии наполнителя, плакированные органическими пленками. [6]
В процессе кислотно-основного взаимодействия важная роль принадлежит образованию молекулярного соединение кислоты с основанием. [7]
В процессе кислотно-основного взаимодействия в апротонном растворителе ионные пары связаны водородной связью. [8]
При протекании процессов кислотно-основного взаимодействия расчет константы устойчивости усложняется. [9]
С процессами сольволиза в растворах тесно связаны процессы кислотно-основного взаимодействия между молекулами растворенного вещества и растворителя, сопровождающиеся ионизацией молекул. [10]
В последние годы важная роль водородной связи в процессах кислотно-основного взаимодействия общепризнана. [11]
Существенным достоинством протолитической теории является учет влияния растворителя на процесс кислотно-основного взаимодействия. [12]
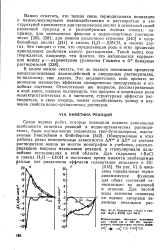 |
Сольволиз f - BuCI в смесях Н25 EtOH при 298 К. [13] |
В целом можно сказать, что до полного понимания процессов кислотно-основных взаимодействий в смешанных растворителях, по-видимому, еще далеко. Это неудивительно, если принять во внимание множество эффектов одновременно оперирующих в подобных системах. Относительно же вопросов, рассматриваемых в этой книге, полезно подчеркнуть, что прогресс в понимании роли неэлектростатических и, в частности, структурных эффектов растворителя, в свою очередь, может способствовать успеху в изучении свойств водно-органических растворов. [14]
При классификации растворителей прежде всего выделяют характер их участия в процессе кислотно-основного взаимодействия. По этому признаку выделяют две большие группы растворителей: апротонные и протолитические. [15]
Страницы: 1 2 3