Введение - атом - фтор
Cтраница 3
Причем оказалось, что воздействие заместителей на экранирование атома углерода, для обоих рядов соединений примерно равно. Это позволило сделать вывод о том, что введение атомов фтора в бензольное кольцо не приводит к изменению механизма передачи влияния заместителя на Сг и С4 атомы углерода бензольного кольца, а имеет место понижение чувствительности к влиянию заместителя атома углерода, связанного с фтором. [31]
Полифосфонитрилхлориды ( NPC12) B известны очень давно, однако многочисленные попытки замещения хлора органическими группами с целью повышения гидролитической устойчивости этих полимеров оставались до последнего времени малоуспешными. В настоящее время переход к более сложным цепям и введение атомов фтора, углеводородных и фторалкильных заместителей открывают новые возможности для поисков полимеров, отличающихся исключительно высокой температурной устойчивостью. [32]
В отсутствие добавок карбанионы исчезают в результате реакции с положительным ионом растворителя, возникшим при радио-лизе, или с микропримесями, присутствующими в растворе. Было найдено, [207, 208], что в случае бензильного карбаниона и его фторпроизводных введение атомов фтора в бензольное кольцо вызывает увеличение периода полупревращения ti / 2 карбаниона. Это находится в согласии с теоретическими основами органической химии. Во-первых, атом фтора обладает отрицательным индукционным эффектом. Очевидно, чем меньше р / С0, тем стабильнее карбанион. [33]
Бензотрифторид не обладает специфическими раздражающими свойствами. Следовательно, введение атома хлора в боковую цепь молекулы толуола приводит к повышению биологической активности соединений на уровне Limac, а введение атома фтора, напротив, уменьшает ее. [34]
Особенно интересные результаты получены при исследовании строения фторсодержащих органических соединений. Так, было показано, что длина связи С-F в монофторидах на 0 05 - 0 06 А больше, чем в полифторидах. В дальнейшем было установлено, что введение атомов фтора изменяет длину соседних связей. [35]
Важную роль в этих процессах играет природа гетероатома бинуклеофиль-ного нуклеофила, поскольку он участвует в образовании и стабилизации промежуточного карбаниона и определяет направление атаки второго нуклеофиль-ного центра по атому углерода как первичной, так и вторичной кратной связи. Направленность этих процессов определяется сочетанием нескольких факторов и позволяет целенаправленно контролировать фазу формирования гетероциклической системы. Именно поэтому такие процессы оказываются наиболее интересными и важными для перфторированных соединений в силу отсутствия таковых для олефинов углеводородного ряда и представляют возможность варьирования свойств в различных функциональных группировках за счет введения атомов фтора. Следует подчеркнуть, что при реакциях перфторолефинов с нуклеофильными реагентами не только происходит конструирование гетероциклического кольца, но и получаются перфторалкильные группы при нем. [36]
Полифторароматические производные элементов VA и VIA подгрупп изучены значительно хуже своих углеводородных аналогов и пока еще не нашли какого-либо значительного использования в практике. Это не удивительно, если иметь в виду, что еще слабо изучена их физиологическая активность, совершенно не исследованы физические свойства. Вместе с тем ясно, что возможности практического использования полифторароматических производных элементов VA и VIA подгрупп могут появиться со временем; по мере увеличения и углубления знаний об этих соединениях. Модификация свойств, обусловленная введением атомов фтора в ароматическое кольцо, позволяет ожидать специфических особенностей, отсутствующих у углеводородных аналогов. Одним из примеров таких особенностей может служить высокая устойчивость N, N-дихлораминов полифторароматического ряда. [37]
Хромоны занимают достойное место в химии гетероциклических соединений. Среди производных хромонов найдены вещества, обладающие биологической активностью и успешно применяемые в медицинской практике. Однако фторсодержащие представители соединений этого класса практически не изучены. В то же время известно, что введение атома фтора в молекулу кардинально изменяет свойства соединений. [38]
Региоселективное замещение водорода на фтор или перфторалкильную группу в гетероциклической системе существенным образом оказывает влияние на биологические и физические свойства молекулы. Как результат в последние годы возросло число работ, направленных на развитие методологии синтеза фторсодержащих гетероциклических соединений с использованием методологии формирования гетероциклов за счет двойной связи перфтороле-фина и бинуклеофильного реагента. Фторолефины являются ключевыми соединениями, на основе которых строится все здание органической химии фтора. Они занимают центральное место в синтетической химии фторорганических соединений. Модификация свойств двойной связи при введении атомов фтора позволяет развить направление реакций, которые отсутствуют в углеводородном ряду, и поэтому создает превосходные возможности для синтеза определенных структур, в том числе и гетероциклических. Они существенно расширяют возможности синтеза гетероциклических соединений, которые могут представить значительный интерес для получения биоактивных соединений для медицины и эффективных препаратов для сельского хозяйства. [39]
Совместно с А. В. Фокиным выполнил ( с конца 1940 - х) комплекс работ, охватывающих вопросы синтеза фторорганических соединений, В 1952 приступил к исследованиям фторолефинов, в результате которых установил электроноамфотер-ный характер двойной связи в их молекулах, исследовал реакции фторолефинов со спиртами, аминами, азидами, меркаптанами. Открыл перегруппировки перфторви-нилкарбинолов во фторангидриды соответствующих кротоновых кислот, бис-трифторметилкетена - во фторангидрид перфторметакрило-вой кислоты, фторированных ал-килазидов - в карбаминофториды. Синтезировал ( 1960 - е) нитро -, амино -, сульфо - и алкоксипроизвод-ные различных фторорганических соединений. Разработал ( 1960 - е) электрохимический метод парциального введения атомов фтора в органические молекулы, с помощью которого получил фторбензол, фтор - и дифторнафталины, фторированные циклоалкадиены и цик-лоалкадиеноны. Развил ( 1964 - 1970) исследования в области химии фторкарбанионов и азанио-нов, приведшие к синтезам многих перфторалкилпроизводных металлов путем замены на металл про-тонирующего водорода в моно-гидроперфторалканах. Решил проблему восстановительной димериза-ции акриловой кислоты гидроди-меризацией ее производных на катализаторе или электрохимическим восстановлением с получением адипонитрила и гексаметилендиа-мина - сырья в производстве волокна нейлон. Создал новые научные направления - химию фторорганических соединений фосфора, серы, селена. [40]
Из таблицы видно, что частоты Ti-ЦПД заметно зависят от природы лигандов при атоме титана. Сдвиги частот могут быть обусловлены как изменением электронных свойств связи Ti-ЦПД ( изменением силового коэффициента) под влиянием лиганда, так и эффектом массы лиганда. Увеличение массы лиганда, согларно теории колебаний, должно привести к снижению частоты. Наиболее четко это влияние видно на примере перехода от циклопентадиенилтитантрихлорида к трибромиду ( сдвиг от 441 к 425 см 1), так как электронные свойства атомов хлора и брома очень близки, сдвиг должен быть в основном обусловлен ростом массы лиганда. Переход от Вг к J приводит к дальнейшему понижению частоты до 415 см-г. Введение атомов фтора, как и следовало ожидать, приводит к существенному росту частоты как за счет уменьшения массы, так и за счет роста акцепторных свойств лиганда. [41]
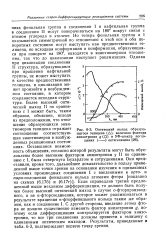 |
Оптический выход образующегося гелицена ( А, величина фактора анизотропии g ( О и УФ-спектр поглощения ( - - - - - - октагелицена. [42] |
Но теперь фенильная группа в I оказывается симметричной по отношению к этой оси и оба поворотных состояния могут выступать как предшественники ге-лицена, но исходная конформация и конформация, образующаяся при повороте на 180, находятся в энантиомерном отношении, так что до циклизации наступает рацемизация. Однако при циклизации соединения II структура, образующаяся при вращении нафтильной группы, не может выступать в качестве предшественника гелицена, и циклизация может произойти в возбужденном состоянии, в котором сохраняется исходная структура. Более высокий оптический выход II по сравнению с I может быть, таким образом, объяснен, исходя из предположения, что отношение образующихся энан-тиомеров гелицена отражает соотношение соответствующих энантиомеров в возбужденных реакционных состояниях. Оставшаяся возможность объяснения, согласно которой результаты могут быть обусловлены более высоким фактором анизотропии у II по сравнению с I, была отвергнута Бухардтом и сотрудниками. Если справедлив третий предложенный выше механизм дифференциации, то должен быть получен более высокий оптический выход в случае о-фторпроизвод-ного, а не n - фторсоединения, которое может рацемизоваться в результате вращения м-фторфенильного кольца таким же образом, как и соединение I. С другой стороны, введение атома фтора не должно существенно изменять фактор анизотропии g, поэтому если дифференциация контролируется фактором анизотропии, то все три соединения должны привести к гелицену с одинаковым оптическим выходом. Результаты, приведенные в табл. 6 - 3, подтверждают первую точку зрения. [43]
Страницы: 1 2 3