Введение - атом - галоген
Cтраница 1
Введение атомов галогенов в кольцо стирола оказывает различное влияние на реакционную способность мономера в зависимости от типа и числа атомов галогена или положения заместителя. [1]
Введение атома галогена в ароматическое ядро представляет собой одну из наиболее важных реакций как в промышленности, так и в лабораторной практике. Эта реакция применима и к ароматическим ге-тероциклам, она легко идет с тиофеном и фураном, но пиридин реагирует намного труднее. [2]
Введение атома галогена в молекулу красителя улучшает чистоту оттенка, повышает яркость красителя и его устойчивость к свету. [3]
Поскольку введение атома галогена в молекулу биологически активного соединения обычно значительно сказывается на величине, а иногда и на характере проявляемой активности, мы поставили задачу получить 2-бромпроизводные некоторых ТГ. [4]
При введении атомов галогена к углероду, несущему нитрогруппу, гидролитическое расщепление а-нитрокетонов облегчается. [5]
Например, введение атома галогена в 9а - положение кортизона ( 1 - 27) повышает активность гормона, удлиняя его период полупревращения. [6]
Как известно, введение атома галогена в а-положение к карбонильной группе циклогексанона вызывает характеристические изменения в спектральных свойствах, зависящие от того, находится ли галоген в аксиальной или экваториальной конформации ( см. разд. В упомянутых работах было проведено сравнение инфракрасных и ультрафиолетовых спектров и дисперсии оптического вращения стероидных кетонов с карбонильной группой в кольце D с аналогичными спектрами их ос-галогенпроизводных с известной конфигурацией галогена. Аксиальный или экваториальный характер атома галогена был выведен на основании полученных данных с использованием закономерностей, установленных для кетонов ряда циклогексана. Полученные результаты показывают, что у 15 - п 17-галогенпроизводных 16-кетостероидов ( 4) 14сс - ряда кольцо D имеет форму полукресла ( 5) ( см. разд. [7]
Галогенирование органических соединений - введение атомов галогена в молекулу, приводящее к образованию связи С-Hal. [8]
Наибольшее значение имеют следующие способы введения атома галогена в молекулу органического соединения: 1) замещение гидроксила на атом галогена при нагревании с концентрированными галоге-новодородными кислотами или с галогенидами фосфора; 2 пои-ссединение галогена или галогенозодорода к двойной ( тройной) связи; 3) прямое замещение водорода на галоген. [9]
Как и в бензильных радикалах, введение атомов галогенов в пара - или лега-положения феноксиметильного радикала почти не изменяет распределение спиновой плотности в кольце. [10]
Фунгицидная активность N-бензоилгидразонов хинонов усиливается при введении атомов галогенов в бензоильный остаток и в хиноидное ядро. Так, 4-хлорбензоилгидразон бензохинона более активен, чем его бензоилгидразон, но уступает по активности бен-зоилгидразону хлорбензохинона. Такое же влияние оказывает введение в ядро хинона метильной группы. Наиболее активным соединением этой группы является бензоилгидразон 2-хлор - 6-метилхи-нона. [11]
Различают два типа атомных групп, ориентирующих введение атома галогена на определенное место в бензольном ядре. [12]
Сопоставление приведенных выше фактов показывает, что введение атома галогена в фенилгерманиевое производное карбонила марганца стабилизирует связь Ge - Мп по отношению к действию брома. [13]
Интересно, что галогензамещенные амиды ведут себя несколько аномально по сравнению с соответствующими кетонами; у них введение атома галогена в а-положении обычно не приводит к сколько-нибудь заметному повышению частоты до тех пор, пока при том же атоме углерода не появляется второй атом галогена, который и вызывает ожидаемое повышение частоты. Последние установили, что такие свойства не являются неожиданными, так как в соответствии с простыми электростатическими представлениями действие обычного мезомерного эффекта у амидов приводит к тому, что у атома азота появляется некоторый формальный положительный заряд. Электростатическое отталкивание между отрицательно заряженными атомами галогена и кислорода усилено, таким образом, электростатическим притяжением между атомами хлора и азота. [14]
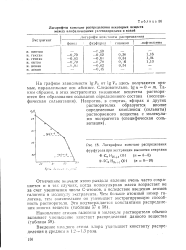 |
Логарифмы констант распределения фурфурола при экстракции высшими спиртами ф. С НаА ОН ( и 4 - 8. [15] |
Страницы: 1 2 3