Прочность - молекула
Cтраница 2
Предполагается, что аномальная прочность молекулы С12 ( Dci - ci 52 ккал / молъ) по сравнению cF2 ( 37 ккал. [16]
Константа диссоциации указывает на прочность молекул в данном растворе. Чем меньше константа диссоциации в данном растворителе, тем слабее диссоциирует электролит и тем, следовательно, устойчивее его молекулы. [17]
По-видимому, это обусловлено прочностью молекулы НС1 и малой ете-пенью его диссоциации в пламени. Бромистый водород в отличие от хлористого, легко диссоциирует; регенерированный свободный бром может снова связывать атомарный водород, обрывая реакционную цепь. Однако не исключено, что и здесь существенны чисто тепловые факторы; легче диссоциирующее бромпроизводное сильнее влияет на температуру горения. [18]
По-видимому, это обусловлено прочностью молекулы НС1 и малой с. Бромистый водород в отличие от хлористого, легко диссоциирует; регенерированный свободный бром может снова связывать атомарный водород, обрывая реакционную цепь. Однако не исключено, что и здесь существенны чисто тепловые факторы; легче диссоциирующее бромпроизводное сильнее влияет на температуру горения. [19]
По-видимому, это обусловлено прочностью молекулы НС1 и малой eje - пенью его диссоциации в пламени. Бромистый водород в отличие от хлористого, легко диссоциирует; регенерированный свободный бром может снова связывать атомарный водород, обрывая реакционную цепь. [20]
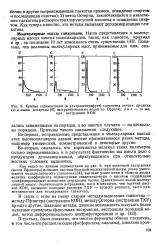 |
Кривые седиментации ( в ультрацентрифуге гликогена печени кролика ( а и мышц аскариды ( б /, экстрагированного водой по Оррелю. в ТА г - то же. [21] |
Во-вторых, оказалось, что прочность молекул таких полимеров сильно переоценивалась и в результате фактически мы имели дело с продуктами деполимеризации, образующимися при относительно жестких условиях выделения. [22]
Тепловой эффект, с которым связана прочность молекул, в подгруппах с увеличением радиуса атомов правильно падает. Так, НС1 - прочное экзотермическое соединение, а Н4РЬ - сильно эндотермическое, крайне непрочное соединение, HF - сильно экзотермическое очень прочное соединение, HI - эндотермическое непрочное соединение. [23]
Это, в свою очередь, увеличивает прочность молекулы ДНК и способствует компактности ее пространственной структуры. [24]
С увеличением числа атомов кислорода в молекулах кислородных кислот прочность молекул увеличивается. Поэтому в безводном состоянии могут существовать хлорная НС1О4, йодноватая НЮ3 и йодная НЮ4 кислоты; все остальные кислородные кислоты галогенов существуют только в водных растворах. [25]
Электрон, находясь между ядрами, притягивается к ним, чем и определяется прочность молекулы. В состоянии г) член, описывающий это охватывающее облако, входит со знаком плюс, а в состоянии ijj - он вычитается. В результате функции г ( и ее квадрат) равны нулю на рассмотренной выше плоскости. [26]
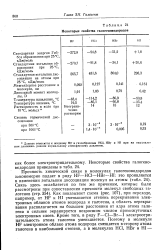 |
Некоторые свойства галогеноводородов. [27] |
Связь здесь ослабляется по тем же причинам, которые были рассмотрены при сопоставлении прочности молекул свободных галогенов ( стр. Как показывает схема ( рис. 107), при переходе, например, от HF к HI уменьшается степень перекрывания электронных облаков атомов водорода и галогена, а область перекрывания располагается на большем расстоянии от ядра атома галогена и сильнее экранируется возросшим числом промежуточных электронных слоев. Кроме того, в ряду F - С1 - Вг-I электроотрицательность атома галогена уменьшается. [28]
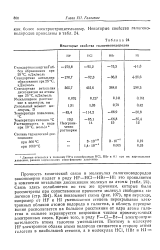 |
Некоторые свойства галогеноводородов. [29] |
Связь здесь ослабляется по тем же причинам, которые были рассмотрены при сопоставлении прочности молекул свободных галогенов ( стр. Как показывает схема ( рис. 107), при переходе, например от HF к HI уменьшается степень перекрывания электронных облаков атомов водорода и галогена, а область перекрывания располагается на большем расстоянии от ядра атома галогена и сильнее экранируется возросшим числом промежуточных электронных слоев. Кроме того, в ряду F - С1 - Вг-I электроотрицательность атома галогена уменьшается. [30]
Страницы: 1 2 3 4