Прочность - связывание
Cтраница 1
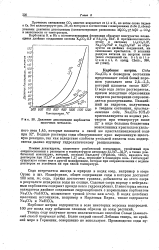 |
Давление диссоциации карбонатов щелочных металлов. [1] |
Прочность связывания С02 заметно возрастает от Li к К, но затем снова падаеэ к Cs. Это иллюстрирует рис. 38, на котором в соответствии с измерениями Лебо ( Lebeau указаны давления диссоциации ( соответствующие равновесию MjC03 5 мЦо -) - COj) в зависимости от температуры. [2]
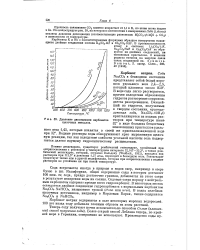 |
Давление диссоциации карбонатов щелочных металлов. [3] |
Прочность связывания С02 заметно возрастает от Li к К, но затем снова падав. Это иллюстрирует рис. 38, на котором в соответствии с измерениями Лебо ( Lebeau) указаны давления диссоциации ( соответствующие равновесию Й СОз L M20 - - С02) в зависимости от температуры. [4]
Прочность связывания в гидратах альдегидов воды различна в зависимости от характера радикалов в различных альдегидах. [5]
Прочность связывания воды в кристаллах может существенно различаться. Некоторые гидраты достаточно устойчивы даже при повышенных температурах. Например, гидратированные сульфаты цинка или никеля обезвоживаются только при температуре выше 280 С. Другие гидраты выветриваются на воздухе: например, дигидрат циануровой кислоты весьма быстро обезвоживается при обычных атмосферных условиях. Вода может удерживаться столь прочно, что в некоторых случаях соответствующие гидраты рассматривают как истинные соединения, в которых все атомы связаны валентными связями: серную кислоту - как гидрат триоксида серы, а гидроксид бария - как гидрат оксида бария. [6]
Прочность связывания СОг заметно возрастает от Li к К, но затем снова падает к Сз. Это иллюстрирует рис. 38, на котором в соответствии с измерениями Лебо ( Lebeau) указаны давления диссоциации ( соответствующие равновесию МаС03 it MjO C02) в зависимости от температуры. [7]
Прочность связывания гидрат-ной оболочки коррелирует с увеличением заряда иона. [8]
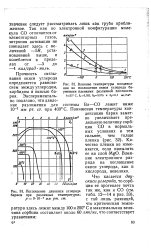 |
Влияние температуры конденсации на поглощение окиси углерода бариевыми пленками различной плотности.| Поглощение двуокиси углерода. [9] |
Прочность связывания окиси углерода определяется равновесием между углеродом, карбидом и окисью бария. Экспериментально показано, что давление разложения для системы Ва-СО лежит ниже 10 - 7 мм рт. ст. при 400 С. [10]
Уменьшение прочности связывания является, кроме того, результатом некомплементарности концевых групп. Так, поли-уридиловая кислота образует двух - и трехцепочечные комплексы с фАфАфАфУ, фАфАфАфАфУ и фАфАфАфАфУф, но они менее стабильны, чем комплексы, образованные соответствующими олиго-нуклеотидами без концевых уридиновых остатков. [11]
В зависимо сти от прочности связывания нитрила на поверхности возрастание v ( CN) будет различным; чем больше рост v ( GN), тем больше, при прочих равных условиях, силовая константа связи азот - атом поверхности. Если же при адсорбции нитрилов ( по крайней мере, алифатических) v ( CN) не будет возрастать, то с большой вероятностью можно заключить, что связь нитрилов с атомами поверхности осуществляется не через атом азота, а каким-то иным способом. [12]
Полная заселенность связи характеризует прочность связывания между двумя атомами: А и В. [13]
Полная заселенность связи характеризует прочность связывания между двумя атомами А и В. [14]
Полная заселенность связи характеризует прочность связывания между двумя атомами: А и В. [15]
Страницы: 1 2 3 4