Прочность - связывание
Cтраница 4
Было предпринято много попыток объяснить действие фитохрома и предлагались различные модели его функционирования. Изменения конформации фитохромного белка при этом, по-видимому, невелики, однако различия в прочности связывания между фитохромом и мембранными структурами для двух форм могут быть значительными. [46]
 |
Влияние фтора на изомеризующую активность 7-оксида алюминия.| Изменение кислотности поверхности 7-оксида алюминия при изменении содержания фтора. [47] |
Способ введения фтора в оксид алюминия оказывает влияние на каталитические и физико-химические свойства алюмоплатинового катализатора. Кроме того, необходимо учитывать простоту и технологичность способа приготовления катализатора в промышленных условиях и прочность связывания фтора с оксидом алюминия. [48]
Наблюдаемое заметное различие в хроматографических характеристиках членов одного и того же ряда ( например, 1-фосфата глюкозы, 6-фосфата глюкозы и 1 6-дифосфата глюкозы) объясняется влиянием величин рК фосфатных групп и константами стабильности боратных комплексных соединений. Кроме того, стерические трудности, создаваемые фосфатной группой, могут снизить стабильность комплексного соединения и, следовательно, снизить прочность связывания, фосфата сахара с анионообменной смолой. [49]
Связывающий характер Зяг-орбитали в какой-то мере теряется из-за взаимодействия с 2аА - орбиталью. Однако в той же мере, в какой утрачивается связывающий характер этой орбитали, возрастает связывающий характер орбитали 2ак, который уже не компенсируется более разрыхляющим характером орбитали 2Ь1ц, так что в целом прочность связывания остается практически той же самой. [50]
Прочность связи кислорода с гемэритрином, как было предложено ранее [40], можно объяснить тем, что два атома железа передают два электрона на антисвязывающие орбитали молекулы кислорода. Очевидно, прочность связи возникающего таким образом пероксо-иона с атомом железа больше, чем у супероксо-иона, который образуется при передаче на О2 только одного электрона. Прочность связывания О2 может быть увеличена также за счет двойной координации молекулы кислорода двумя атомами железа. С другой стороны, гемэритрин устойчив по отношению к окислению, что, по-видимому, обеспечивается главным образом природой белковой цепи, окружающей активный центр. [51]
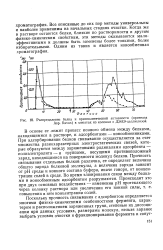 |
Распределение белка и протеолитической активности ( протеаза Asp. flavus в элюатах из колонки с ДЭАЭ-целлюлозой. [52] |
В основе ее лежит процесс ионного обмена между белками, находящимися в растворе, и адсорбентами - ионообменниками. При адсорбировании белков связывание осуществляется за счет множества разнохарактерных электростатических связей, которые образуются между заряженными радикалами адсорбента - лолиэлектролита - и группами, несущими противоположный заряд, находящимися на поверхности молекул белков. Прочность связывания отдельных белков различна, ее определяет величина общего заряда белковой молекулы, а величина заряда зависит от рН среды и ионного состава буфера, иначе говоря, от концентрации солей в среде. Во время элюирования связи между белками и ионообменным адсорбентом разрушаются. [53]
Фракционирование белков на гидроксиапатите [23, 24] или геле фосфата кальция [25] является особой разновидностью ионообменной хроматографии. Микрокристаллические частицы ГА состава Саю ( РО4) б ( ОН) 2 или гель фосфата кальция фиксированы обычно на инертном носителе, например целлюлозе. На прочность связывания положительно заряженных группировок оказывают сильное влияние неорганические соли; прочность связывания отрицательно заряженных групп практически не зависит от концентрации солей. Кроме того, сорбция в присутствии солей зависит и от молекулярной массы белка. [54]
Следует отметить, что асфальтеновые молекулы в природных нефтях, как правило, не полностью реализуют все свои координационные возможности по связыванию ионов металлов. Устойчивость образующихся при этом комплексов, вероятно, существенно ниже, чем патпвных, поскольку в процессе формирования состава нефтей ионы металлов должны связываться с наиболее выгодными в энергетическом отношении лигандными центрами. Правда, специальных исследований по выяснению прочности связывания металлов, насколько нам известно, не проводилось. [55]
Фракционирование белков на гидроксиапатите [23, 24] или геле фосфата кальция [25] является особой разновидностью ионообменной хроматографии. Микрокристаллические частицы ГА состава Саю ( РО4) б ( ОН) 2 или гель фосфата кальция фиксированы обычно на инертном носителе, например целлюлозе. На прочность связывания положительно заряженных группировок оказывают сильное влияние неорганические соли; прочность связывания отрицательно заряженных групп практически не зависит от концентрации солей. Кроме того, сорбция в присутствии солей зависит и от молекулярной массы белка. [56]
Страницы: 1 2 3 4