Прочность - комплексное соединение
Cтраница 3
При этом функция Т носит название связующей орбитали и характеризует более устойчивое состояние орбитали и прочность комплексного соединения. Функция W соответствует случаю разрыхляющей орбитали. [31]
Применение электромиграционного метода для исследования состояния веществ в растворе ( определение заряда и радиуса ионов, прочности комплексных соединений и ассоциатов) основывается на наблюдении за подвижностью изучаемых компонентов. Подвижность является сложной функцией состава и размеров иона, а также состава и состояния раствора. Факторы, влияющие на подвижность ионов, можно разделить на две не очень строго различимые группы: химические и физические. К химическим факторам можно отнести процессы, происходящие непосредственно в сфере воздействия иона: диссоциацию и ассоциацию ионов водорода, гидро-ксила и лигандов, связывание молекул воды в гидрат-ной оболочке. К физическим факторам относится изменение потенциальной энергии ионов вследствие воздействия электрических полей окружающих ионов, изменение активности воды с изменением концентрации электролита, влияние температуры. [32]
Резюмируя, можем сказать, что энергия гидратации является только одним из факторов, влияющих на прочность комплексных соединений в растворе, причем при данном центральном атоме нужно учитывать как энергию гидратации аддендов, так и энергию гидратации комплексных ионов. [33]
Образование селективных минералов связано с уменьшением ионного радиуса в ряду РЗЭ от La к Lu, что изменяет прочность комплексных соединений в том же направлении, благодаря чему в природе РЗЭ перераспределяются и избирательно концентрируются в минералах. Влияние размеров ионных радиусов сказывается и в избирательности изоморфного замещения ионами РЗЭ ионов других металлов. Так, в минералах с крупными катионами ( Sr, Ba, Th) последние замещаются элементами преимущественно цериевой подгруппы, в минералах с небольшими катионами ( Mn, Fe, U, Zr) - катионами элементов иттриевой подгруппы. Известно лишь очень немного минералов, содержащих РЗЭ без резкого преобладания подгрупп. [34]
Количественная характеристика экстракции элемента из растворов минеральных кислот зависит от его состояния в растворе данной кислоты и от прочности комплексных соединений с ее анионом. [35]
Образование селективных минералов связано с уменьшением ионного радиуса в ряду РЗЭ от La к Lu, что изменяет прочность комплексных соединений в том же направлении, благодаря чему в природе РЗЭ перераспределяются и избирательно концентрируются в минералах. Влияние размеров ионных радиусов сказывается и в избирательности изоморфного замещения ионами РЗЭ ионов других металлов. Так, в минералах с крупными катионами ( Sr, Ba, Th) последние замещаются элементами преимущественно цериевой подгруппы, в минералах с небольшими катионами ( Mn, Fe, U, Zr) - катионами элементов иттриевой подгруппы. Известно лишь очень немного минералов, содержащих РЗЭ без резкого преобладания подгрупп. [36]
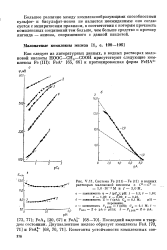 |
Система Fe ( III-Fe ( II в водных растворах малоновой кислоты с С СГ 1 0 - 10 - 4М и / 3 0 М. [37] |
Большое различие между комплексообразующими способностями сульфат - и бисульфат-ионов не является неожиданным: оно согласуется с эмпирическим правилом, в соответствии с которым прочность комплексных соединений тем больше, чем больше сродство к протону лиганда - аниона, сопряженного с данной кислотой. [38]
Малые значения ее ( ne / rzl) снижают способность к омплексообразованию, большие ( ne / rz 0 - 15) приводят к увеличению прочности комплексного соединения. Если связь между центральным атомом и лиган-дами обусловлена в основном электростатическим фактором, то в главных подгруппах способность к комплек-сообразованию должна уменьшаться сверху вниз. [39]
Из виннокислого раствора протактиний ( IV) не осаждается ни аммиаком, ни щелочью, а из лимоннокислого раствора осаждается только едким натром, что характеризует прочность комплексных соединений с этими кислотами. [40]
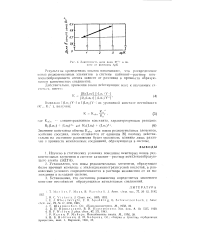 |
Зависимос П, доли иона Рг3 в ио-иите от величины ДрК. [41] |
Значение константы обмена К0бм для ионов редкоземельных элементов, особенно соседних, мало отличается от единицы Ш, поэтому действительно на состояние равновесия будет оказывать влияние лишь различие в прочности комплексных соединений, образующихся в системе. [42]
В каждой паре этих соединений происходит понижение частоты валентных колебаний v3 сульфатной группы, свидетельствующее об упрочнении связи лиганда с атомом - титана при переходе от К к NH и от Rb к Cs, что согласуется с представлением о влиянии внешнесферного катиона на прочность комплексного соединения с одинаковой внутренней сферой. [43]
Для некоторых РЗЭ эти соединения были выделены в твердом виде. Прочность комплексных соединений в нейтральных растворах настолько велика, что они не разрушаются при добавлении оксалата, а из щелочных растворов даже ион фтора не выделяет осадка, несмотря на малую растворимость фторидов РЗЭ. [44]
Во всех случаях комплексообразования с остатками неорганических и органических кислот или нейтральными молекулами рзэ и иттрий в трехвалентном состоянии обнаруживают координационную емкость, равную шести. Прочность комплексных соединений существенно зависит также от рН среды и, как правило, уменьшается с увеличением кислотности. [45]
Страницы: 1 2 3 4