Дивинилсульфид
Cтраница 2
В неводных средах параллельно может происходить де-гидрохлорирование с образованием дивинилсульфида. Медленно гидролизуется водой ( в насыщ. Легко реагирует в неводных средах с тиосуль-фатами, солями карболовых к-т, алкоголятами и фенолятами щелочных металлов с образованием нетоксичных продуктов. Окисляется до с льфоксида и сульфона. [16]
Смесь свежеперегнанных 2 58 г ( 0 03 моля) дивинилсульфида и 3 72 г ( 0 06 моля) этантиола нагревают в запаянной ампуле объемом 25 мл в течение 18ч при 65 - 70 С, затем смесь фракционируют в вакууме. [17]
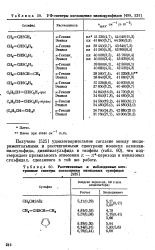 |
УФ-спектры поглощения винилоульфидов.| Рассчитанные и наблюдаемые электронные спектры поглощения виниловых сульфидов f [ 52o ]. [18] |
Получено [525] удовлетворительное согласие между экспериментальными и рассчитанными спектрами молекул алкилви-нилсульфида ( дивинилсульфида и тиофена ( табл. 60), что подтверждает правильность отнесения п - я - перехода в виниловых сульфидах, сделанного в той же работе. [19]
 |
УФ-спектры поглощения винилоульфидов.| Рассчитанные и наблюдаемые электронные спектры поглощения виниловых сульфидов. [20] |
Получено [525] удовлетворительное согласие между экспериментальными и рассчитанными спектрами молекул алкилви-нилсульфида ( дивинилсульфида и тиофена ( табл. 60), что подтверждает правильность отнесения л - п - перехода в виниловых сульфидах, сделанного в той же работе. [21]
Получают аналогично N 32 из 2 58 г ( 0 03 моля) дивинилсульфида и 4 57 г ( 0 06 моля) пропантиола ( синтез см. № 1) 5 гди ( 2-пропилтиоэтил) - сульфида, выход 72 % ( см. примечание к № 35), т.кип. 140 С / 1 мм, т.пл. 27 - 28 С. [22]
А -, Гаврилова Г. М., Калабин Г. А. и др. Циклоприсоеди - т; нение дивинилсульфида к тиомочевине. [23]
Крахмален, , Кушников Ю. А., Светлов А. К. и др. Инфракрасные спектры и строение полимеров дивинилсульфида. [24]
Когда неочищенный ацетилен нагнетают в ацетон в пористой среде, большая часть РН3 [14, 15] и дивинилсульфида [15] удерживается этой средой. При содержании в исходном газе 40 - 50 мг / м3 такое сокращение является еще более резким: 42, 29 и 26 % соответственно при 8, 20 и 32 С. [25]
Ацетилен из сухих генераторов содержит серу в виде меркаптанов и, главным образом, в виде дивинилсульфида. [26]
Тиофен в различные периоды его истории был известен под названиями: тиофуран, тиол, тиотетрол и дивинилсульфид. Так как для различных производных тиофена часто применяют названия, содержащие необычные приставки и суффиксы, очевидно, чуждые самому этому соединению, номенклатура для соединений этого класса еще окончательно не установлена; отсутствуют исчерпывающие правила или нормы, определяющие ее. [27]
Тиофен в различные периоды его истории был известен под названиями: тиофуран, тиол, тиотетрсл и дивинилсульфид. Так как для различных производных тиофена часто применяют названия, содержащие необычные приставки и суффиксы, очевидно, чуждые самому этому соединению, номенклатура для соединений этого класса еще окончательно не установлена; отсутствуют исчерпывающие правила или нормы, определяющие ее. [28]
Единственным доводом в пользу высказанного предположения авторы считают наблюдаемый ими факт более легкой циклизации этилви-кил - и дивинилсульфидов, чем диэтилсульфида. Однако это различие может быть обусловлено и другими причинами, например протеканием реакции с иной лимитирующей стадией или тем, что быстрее идет процесс димеризации непредельных углеводородных фрагментов, чем насыщенных, и др. Образование непредельных тиоэфиров хотя термодинамически и возможно, представляется маловероятным при повышенной температуре вследствие большой разницы в прочности связей С-S и С - Н в тиоэфирах ( см. табл. 52, с. Возникновение гомологов тиофена, которые не должны получаться при внутримолекулярной циклизации тноэфиров, объясняется авторами протеканием различных реакций. Одним из возможных направлений они считают циклизацию дпалкил-сульфидов, получающихся в результате взаимодействия продуктов крекинга исходного тиоэфира - сероводорода или меркаптана и олефинов. Особенно вероятно, по мнению авторов, возникновение алкилтиофенов из тиоэфиров вследствие протекания полимеризационно-деполимеризацион-ных процессов, которым предшествует образование непредельных тиоэфиров. [29]
Как следует из данных по реакции тиомочевины с ацетиленом [ 14Г, 265 ], увеличение концентрации ацетиленового компонента приводит к повышению выхода дивинилсульфидов. При 7-кратном избытке ацетилена выход ДВС превышает 80 %, тогда как при эквимольном соотношении в тех же условиях. [30]
Страницы: 1 2 3 4