Биосинтетические пути
Cтраница 2
Что же касается перечисленных здесь других ну-клеозид-5 - трифосфатов, то все они выполняют специализированные функции, обслуживая только строго определенные биосинтетические пути. Свои концевые фосфатные группы они получают от АТР в реакциях, катализируемых Mg2 - зависимыми ферментами, которые носят название нуклеозиддифосфокиназ. [16]
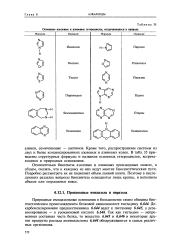 |
Основные азоловые и азиновые гетероциклы, встречающиеся в природе. [17] |
Относительно биогенеза азоловых и азиновых производных можно, в общем, сказать, что к каждому из них ведут многие биосинтетические пути. Подробно рассмотреть их не позволяет объем данной книги. Поэтому в последующих разделах вопросы биосинтеза освещаются лишь кратко, в неполном объеме или опускаются вовсе. [18]
Как было показано выше на примере грибных алкалоидов эхи-нулина ( 11) и агроклавина ( 12) [25], существуют биосинтетические пути, в которых участвуют различные предшественники; структурный анализ этих соединений не представляет затруднений. Менее очевидно доказанное участие триптофана и мевалоно-вой кислоты в биосинтезе большой и сложной в структурном отношении группы растительных индольных алкалоидов. [19]
Корни гермакранового древа образованы катионом 2.146, гермакреном А 2.177 и другими гермакрадиенами и - триенами. Биосинтетические пути, очерченные ранее схемами 26 и 29, составляют главные ветви. Они были выделены особо и описаны более подробно, так как принадлежащие к ним соединения количественно превалируют среди С15 - изопреноидов. Однако почти все из этих путей имеют продолжение и разделяются на более тонкие ответвления. Для упрощения в них даны только обозначения образующихся и разрывающихся С-С связей и игнорируются механизмы идущих при этом химических реакций. [20]
Сплошные стрелки указывают те реакции цикла восстановления углерода, которые были выяснены Кальвином и его сотрудниками. Двойными стрелками отмечены некоторые биосинтетические пути, ведущие свое начало от промежуточных соединений цикла. Звездочками указана относительная степень включения метки ( приближенно) после нескольких секунд фотосинтеза, определенная методом химической деградации, как указано в тексте. Цифры у стрелок - это номера уравнений реакций, приведенных в тексте; римские цифры при структурных формулах те же, что ив тексте. [21]
 |
Реакция трансаминирования. Переносимая аминогруппа выделена красным. В большей части реакций трансаминирования акцептором аминогрупп служит а-кетоглутарат. [22] |
Итак, общим акцептором, принимающим аминогруппу от большинства аминокислот, является а-кетоглутарат. Образовавшийся L-глутамат служит для того, чтобы направлять аминогруппы на определенные биосинтетические пути ( гл. Это означает, что величина ДО0 для таких реакций близка к нулю ( разд. [23]
Таким образом, анализируя биосинтетические схемы образования различных фенольных производных, мы видим, что жесткой привязанности химического класса природных соединений к одному биосинтетическому пути нет - шикиматныи и поликетидныи пути синтеза используются здесь как бы в сопряженном варианте. А если принять во внимание существование изопрено-идных фенольных соединений, то мы уже обязаны учитывать, как минимум, три сопряженных биосинтетических пути: шикиматныи, поликетидныи и мевалоновый. [24]
Биосинтетические пути и соответствующие им катаболические пути контролируются разными регуляторными ферментами. Обычно регуляция соответствующих биосинтетических и катаболи-ческих путей осуществляется координированным образом, реципрокно, так что стимулирование биосинтетического пути сопровождается подавлением катаболи-ческого пути, и наоборот. Более того, биосинтетические пути регулируются обычно на одном из первых этапов. Это избавляет клетку от непроизводительных трат: она не расходует предшественники на синтез тех промежуточных продуктов, которые ей не понадобятся. Мы вновь убеждаемся на этом примере, что принцип экономии лежит в основе молекулярной логики живых клеток. [25]
Пиридиновое ядро входит в состав многих конденсированных алкалоидных молекул. Несмотря на простоту структуры, биосинтетические пути к ним сложны, многообразны и часто не до конца выяснены. В живой природе существуют, по крайней мере, четыре основных способа конструирования пиридиновых молекул. По одному из них непосредственным предшественником пиридинов выступают участники первичного метаболизма. Именно так растения и бактерии из фосфоглицеринового альдегида и аспарагиновой кислоты синтезируют пиридин - 3-карбоновую кислоту 6.130, именуемую никотиновой. Основные этапы рождения этой молекулы показаны на схеме ИЗ. [26]
Тетрагидро - и дигидропирролы называются соответственно пирролиди-ном и пиррол ином. Их неконденсированные производные составляют собой относительно небольшую группу природных оснований. Несмотря на простоту химического строения, биосинтетические пути, ведущие к отдельным их представителям, весьма многочисленны и различны. Наиболее простые пирролидины происходят от аминокислоты пролина ( разд. Это стахид-рин 6 92, бетоницин 6.93 и М - этоксикарбонил - Ь - пролинамид 6.94. Первые два найдены во многих видах растений, в частности, в табаке, лкшерне, тысячелистнике. Амид 6.94 обнаружен в листьях Arnica montana. Сам пролин образуется из небелковой кислоты орнитина, которая дает начало нескольким биосинтетическим последовательностям ( см. разд. Одна из них ведет к пролину и упомянутым выше простым алкалоидам. По другому пути через путресцин 6.21 генерируется реакционноспособный катион N-метил-пирролиния 6.95, который играет важную роль в биогенезе многих алкалоидов, содержащих пирролидиновые кольца. [27]
Настоящий раздел представляет собой введение в изучение биосинтеза и поэтому его первейшая задача заключается в рассмотрении самых общих вопросов предмета. Результатом развития этой сравнительно новой научной дисциплины является понимание путей происхождения природных соединений и взаимосвязей между ними ( часто довольно простых, но иногда интригующе запутанных), которые будут проиллюстрированы ниже на ряде примеров. В последующих главах несколько более детально описаны биосинтетические пути, ведущие к основным индивидуальным классам природных соединений. [28]
Одна из наиболее разветвленных ветвей вторичного метаболизма представлена изопреноидами. Происхождение названия и первые этапы биосинтеза этого класса веществ уже обсуждались ( см. разд. Упомянутые в нем простейшие углеводороды и спирты под действием ферментных систем живой природы могут подвергаться реакциям циклизации, окисления, восстановления, перегруппировки и многим другим, образуя чрезвычайно богатые числом членов группы веществ, играющих важную роль в жизнедеятельности производящих их организмов. Биосинтетические пути, ведущие к изопреноидам, функционируют, кроме растений, у грибов, водорослей, беспозвоночных и позвоночных животных, т.е. практически на всех уровнях организации живой материи. По мере подъема по эволюционной лестнице удельная роль изопреноидного метаболизма, в общем, уменьшается. Тем не менее, даже у млекопитающих такие изопреноиды, как холестерин, стероиды, долихолы, убихиноны составляют важный компонент их биохимического устройства. [29]
 |
Влияние негативного ( ЦТФ и позитивного ( АТФ эффекторов на кинетические характеристики ( Ктах и Км аспартаткарбамоилтранс.| Схема ковалентной модификации гликогенфосфорилазы из. [30] |
Страницы: 1 2 3