Пятиокись - ниобий
Cтраница 2
Пятиокись ниобия, полученная ионным обменом, содержала менее 0 002 % TiCb и менее 0 05 % TaaOs; содержание тантала в чистой пяти-окиси ниобия следует считать завышенным из-за недостаточной чувствительности примененного метода анализа. [16]
Пятиокись ниобия начинает взаимодействовать с хлором только при температурах выше 700 С. В результате хлорирования окислов в присутствии восстановителей при температурах ниже 500 С образуются преимущественно оксихлориды, а в интервале 500 - 1000 С получают смесь хлоридов и оксихлоридов. Если продукты реакции вместе с избытком хлора пропустить через слой угля, нагретого до 500 С, можно получить пентахлориды, практически свободные от оксихлоридов. [17]
Пятиокиси ниобия и тантала предварительно прокаливались при t 500 до постоянного веса и тщательно измельчались в агатовой ( фторопластовой) ступке или в агатовой шаровой мельнице. [18]
Раствор пятиокиси ниобия с содержанием 0 5 мг NbjOs в 1 мл, готовят следующим образом: 0 1000 г пятиокиси ниобия помещают в стакан вместимостью 100 мл я растворяют при нагревании в 20 мл серной кислоты и 2 г сернокислого аммония. Раствор охлаждают, переносят в мерную колбу вместимостью 200 мл и доводят до метки серной кислотой. Титр полученного раствора устанавливают весовым куп-фероновым методом. [19]
Получение пятиокиси ниобия основано на экстракционном разделении фторидных комплексов ниобия и тантала. Тантал экстрагируется при значительно более низкой концентрации HF ( 0 8 - 1 / И), чем ниобий, что делает возможным их разделение при экстракции циклогексаноном. В этих условиях ниобиевая кислота превращается в кристаллическую соль пероксиниоби-ата аммония состава ( МН4) з) МЬОв, примеси же остаются в растворе. [20]
Примесь пятиокиси ниобия к танталу в циклогексаноне может быть снижена до 0.1 % и ниже. [22]
Плав пятиокиси ниобия обрабатывают 10 % - ным раствором винной кислоты, а плав двуокиси титана - разбавленным ( 1: 15) раствором серной кислоты и работают далее с растворами. [23]
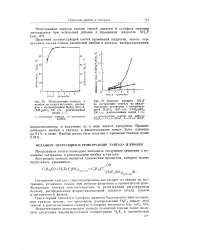
Взаимодействие пятиокиси ниобия с хлоралюминатом натрия в сопоставимых условиях начинается при температурах на 300 град ниже, чем с пятиокисью тантала. В табл. 89 приведено давление пара NbOCl3 и ТаС15, соответствующее равновесию при различных температурах. [24]
Количество пятиокисей ниобия и тантала в исследуемом растворе не должно превышать количество осаждающего реактива на угле. [25]
Навеску пятиокиси ниобия 0 1 - 0 2 г растворяют, как описано выше, упаривают раствор до объема 3 - 5 мл, разбавляют до 80 мл водой, нейтрализуют раствор аммиаком до рН 1 2 ( по универсальной индикаторной бумажке) и прибавляют раствор таннина. Осадку дают отстояться 3 - 5 часов, затем отфильтровывают, отмывают на фильтре 3 - 4 раза водой. Фильтр с осадком подсушивают, сжигают и прокаливают при 1000, как описано выше. [26]
При нагревании пятиокись ниобия слегка желтеет, пятиокись тантала не изменяется. Пятиокиси растворяются в горячей концентрированной фтористо-водородной кислоте, а также при сплавлении с щелочными пиросульфатом, карбонатом и едкой щелочью. При обработке пиросульфатного сплава горячей водой или разбавленными кислотами выделяется осадок земельных кислот; обработка пиросульфатного сплава винной или щавелевой кислотой, напротив, дает прозрачный раствор тартратных или оксалатных комплексов земельных кислот. Сплав с углекислым или едким калием растворяется в воде с образованием раствора ниобата или танталата калия. После сплавления с углекислым или едким натром и выщелачивания водой остается осадок нерастворимых ниобата и танталата натрия. [27]
Сложные реакции пятиокиси ниобия с сульфатом, бисульфатом, пиросульфатом калия и с сульфатом аммония, объясняемые теорией Люкса-Флуда. [28]
Голубые кристаллы пятиокиси ниобия при нагревании в присутствии воздуха становятся бесцветными, не теряя при этом монокристалличности. [29]
Исходная навеска пятиокиси ниобия 25 г. Гидрид кальция берут в 50 % - ном избытке против теоретически рассчитанного. Смесь исходных компонентов загружают в закрытую с одного конца муллито-вую трубку или муфель из нержавеющей стали и вставляют в горизонтальную печь сопротивления. Муфель откачивают примерно до 100 мк и включают нагрев печи. При медленном нагреве печи при 450 С давление резко повышается, что связано с началом разложения гидрида кальция. После охлаждения реакционный спек высыпают малыми порциями в холодную воду, которая реагирует с ним с выделением пузырьков газа. Порошок затем промывают разбавленной соляной кислотой для удаления кальция и окиси кальция, каждый раз увеличивая концентрацию. [30]
Страницы: 1 2 3 4