Дигидрид
Cтраница 1
Дигидрид дибутил германия [26-28] присоединяется при 100 С к молекуле фенилацетилена, образуя гидрид дибутилстирилгермания ( C4He) 2Ge ( H) CHCHCeH5, который при продолжительном нагревании образует полимер в виде желтого масла. [1]
Дигидриды удобнее всего использовать для восстановления простейших альдегидов и кетонов, с которыми реакции проходят гладко и с хорошим выходом. [2]
Дигидрид тегракарбонила железа устойчив в щелочных средах, но легко разлагается в присутствии кислот. Химическая связь в нем, по мнению Бланчарда и Виндзора [440], осуществляется за счет привлечения валентных электронов водорода для укомплектования J-уровней атома железа. Водород в гетракарбонилдигядриде железа имеет слабокислый характер. Это давало основание считать, что - его связь с железом осуществляется через кислород [ 441, стр. [3]
Дигидрид полония, РоН2, образуется при действии водорода на нагретый до 700 металлический полоний. [4]
Дигидрид диметилолова не реагирует с этиленом при нагревании смеси реагентов до 50 С в защищенной от действия света ампуле в течение 180 час. Реакция начинает протекать с заметной скоростью, если смесь облучать УФ-светом. В этих условиях из эквимолекулярных количеств дигид-рида диметилолова и этилена образуются неустойчивый гидрид диметил-этилолова и диметилдиэтилолово с выходом 37 и 31 % соответственно. [5]
Дигидрид тетра-н-бутилдистаннана приготовлен [56] восстановлением соответствующего дихлорида литийалюминийгидридом в эфире. При обработке этого соединения уксусной кислотой выделяется рассчитанное количество водорода и образуется со. Подобным образом получены [48] и другие гидриды этого типа. [6]
Дигидрид ди-н-бутилолова реагирует с окисью ди-н-бутилолова примерно за 12 час. [7]
Полученный дигидрид представляет собой хрупкое вещество, сохраняет металлический блеск, легко растирается в порошок. [8]
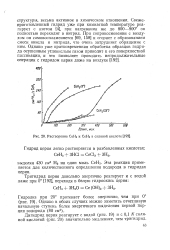 |
Растворение СеН2 и СеНз в соляной кислоте. [9] |
Дигидрид церия реагирует с водой ( рис. 19) и с 0 1 N соляной кислотой ( рис. 20) значительно медленнее, чем тригидрид. [10]
Дигидрид плутония РиН2 имеет гранецентрированную кубическую решетку CaF2 с а5 359 А. [11]
Органические дигидриды германия получают аналогично моногидридам, исходя из двугалоидных соединений германия. [12]
Мономерные дигидриды состава ( я - С5Н5) 2МН2, где М Ti, Zr или Hf, неизвестны; однако спектры ЭПР подтверждают существование парамагнитного димера [ ( я - С5Н5) 2Т1 - р - Н ] 2 ( гл. [13]
Прочным дигидридом является этан С2Н, остальные весьма неустойчивы. [14]
Некоторые дигидриды очень легко изомеризуются, так что убедительно доказать положение двойных связей часто невозможно. В настоящем обсуждении приведены структуры, данные отдельными исследователями. Хотя эти структуры не определены во всех подробностях, они, по-видимому, в общем согласуются с известными фактами. Дигидропиразины с двумя заместителями у одного и того же атома углерода ядра вполне устойчивы к окислению, тогда как такие, в которых этот тип замещения отсутствует, легко превращаются в соответствующие пиразины. Это осуществляется нагреванием или воздействием воздуха при комнатной температуре. При кислом гидролизе Дигидропиразины расщепляются по связям C N. Однако на промежуточной стадии может происходить изомеризация, так что продукты гидролиза не обязательно будут те, которые можно предсказать на основании первоначальной структуры ди-гидропиразина. [15]
Страницы: 1 2 3 4