Дигидронафталин
Cтраница 1
Дигидронафталин не присоединяет альдегидной группы. Стирол характеризуется пониженной реакционной способностью; кроме того, в условиях оксо-реакции он полимеризуется и лишь в наиболее благоприятных случаях дает ( и то не более 10 - 20 %) фонилпропанол. [1]
Дигидронафталин [40, 281] и 1-метил - 1 2-дигидронафталин [282] окисляются в жидкой фазе в соответствующие гидроперекиси. [2]
Дигидронафталин [40, 281] и 1-метил - 1 2-дигидронафталин 1282 ] окисляются в жидкой фазе в соответствующие гидроперекиси. [3]
Дигидронафталин не присоединяет альдегидной группы. [4]
Дигидронафталин при нагревании с этилатом натрии превращается в 1 2-дигидронафталин, являющийся, следовательно, более устойчивым из этих двух изомеров. [5]
Дигидронафталин при нагревании с этилатом натрия превращается в 1 2-дигидронафталин, являющийся, следовательно, более устойчивым из этих двух изомеров. [6]
Дигидронафталин полимеризуется под действием серной кислоты. [7]
Окисление дигидронафталина, естественно, должно дать соответствующую перекись, последняя же с отщеплением частицы воды должна превратиться в а-нафтол. [8]
Оба изомерных дигидронафталина легко присоединяют одну молекулу брома. [9]
Диальдегид, полученный озонолизом дигидронафталина [ реакция ( 3) 1, может циклизоваться только с образованием 2-инденальде-гида. Реакция ( 4) является частью схемы синтеза стероидов по Гарварду. Диальдегид в этом случае получают гидроксилированием кратной связи четвертого конденсированного ядра с последующим периодатным расщеплением ш - диола. В полученном таким образом соединении ( III) две альдегидные группы неэквивалентны, и при внутримолекулярной атаке карбаниона продукт ( IV) образуется с большим выходом, чем продукт ( V), так как подход молекулы основания к сс-атому углерода, обведенному на схеме кружком, менее затруднен. [10]
Диальдегид, полученный озонолизом дигидронафталина [ реакция ( 3) 1, может циклизоваться только с образованием 2-инденальде-гида. Реакция ( 4) является частью схемы синтеза стероидов по Гарварду. Диальдегид в этом случае получают гидроксилированием кратной связи четвертого конденсированного ядра с последующим периодатньш расщеплением виц-днола. В полученном таким образом соединении ( III) две альдегидные группы неэквивалентны, и при внутримолекулярной атаке карбаниона продукт ( IV) образуется с большим выходом, чем продукт ( V), так как подход молекулы основания к ос-атому углерода, обведенному на схеме кружком, менее затруднен. [11]
Дальнейшие опыты показали, что фенилзамещенные дигидронафталины, содержащие в фенильном радикале орто-заместители, не вступают в диеновый синтез. Так, например, оказалось, что 1 - ( о-толил) - и 1 - ( о-анизил) - 3 4-дигидронафталины ( XV; R СНз, СНзО) не дают аддуктов в самых различных условиях, что, по-видимому, объясняется нарушением ( под влиянием заместителя R) копланарности циклов, содержащих диеновую систему. [12]
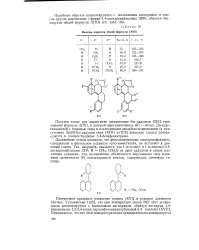 |
Выходы аддуктов общей формулы ( XIII. [13] |
Дальнейшие опыты показали, что фенилзамещенные дигидронафталины, содержащие в феыильном радикале орто-заместители, не вступают в диеновый синтез. Так, например, оказалось, что 1 - ( о-толил) - и 1 - ( о-анизил) - 3 4-дигидронафталины ( XV; R СНз, СНзО) не дают аддуктов в самых различных условиях, что, по-видимому, объясняется нарушением ( под влиянием заместителя R) копланарности циклов, содержащих диеновую систему. [14]
Приводимое описание получения бутадиена и дигидронафталина может дать представление об условиях превращения дибромпроизводных в непредельные соединения при действии цинка в спиртовой среде. [15]
Страницы: 1 2 3 4