Атомный ионный радиус
Cтраница 1
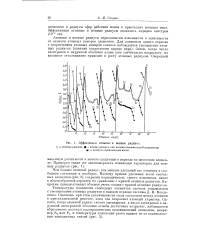 |
Эффективные атомные F ионные радиусы. [1] |
Атомные и ионные радиусы периодически изменяются в зависимости от величин атомных номеров элементов. Затем, когда число электронов в наружной оболочке атома уже значительно возрастает, их взаимное отталкивание приводит к росту атомных радиусов. [2]
Атомные и ионные радиусы строго следуют закономерности, лежащей в основе периодического закона Д. И. Менделеева: существует определенная связь между положением элемента в периодической системе и эффективными радиусами его атомов и образуемых им ионов. [3]
Атомные и ионные радиусы на рисунках также пропорциональны кажущимся атомным и ионным радиусам в кристаллах, а именно увеличены в 12 000 000 раз. [4]
Атомные и ионные радиусы для химических элементов приведены в справочной литературе. [5]
Атомные и ионные радиусы на рисунках также пропорциональны кажущимся атомным и ионным радиусам в кристаллах, а именно увеличены в 12 000 000 раз. [6]
Атомные и ионные радиусы строго следуют закономерности, лежащей в основе периодического закона Д. И. Менделеева: существует определенная связь между положением элемента в периодической системе и эффективными радиусами его атомов и образуемых нм ионов. [7]
Атомные и ионные радиусы так же периодически меняются с увеличением заряда ядра. Из сопоставления ( рис. 56, а и рис. 56, б) видно, что минимальным значениям / у щелочных металлов соответствуют максимальные значения радиусов. [8]
 |
Атомные и ионные радиусы химических элементов. [9] |
Атомные и ионные радиусы имеют важное значение для характеристики кристаллических решеток простых веществ и химиче-ских соединений, в особенности при изучении явлений сорбции, изоморфизма и соосаждения. [10]
 |
Потенциалы ионизации рения и некоторых сходных с ним элементов. [11] |
Атомные и ионные радиусы рения близки к радиусам молибдена, вольфрама, осмия, иридия и других платиновых металлов. [12]
Атомные и ионные радиусы элементов также изменяются периодически с возрастанием порядкового номера. Максимальные величины для этих параметров приходятся на щелочные металлы. В вертикальном направлении сверху вниз величина атомных и ионных радиусов возрастает. Четкая закономерность прослеживается для многих других физических и химических свойств элементов, например атомных объемов, внешнего вида, кристаллической структуры, температур плавления, коэффициентов линейного расширения и объемной сжимаемости в кристаллическом состоянии, характера окислов, водородных соединений, окислительно-восстановительных свойств элементов, их комп-лексообразования. [13]
Атомные и ионные радиусы циркония и гафния практически одинаковы, поэтому очень похожи и их химические свойства. Обычна наблюдаются лишь очень малые различия, например в растворимости или летучести соединений. [14]
 |
Физические свойства металлов главной подгруппы II группы. [15] |
Страницы: 1 2 3 4