Атомный ионный радиус
Cтраница 3
Как видим, атомные и ионные радиусы технеция и рения близки ( следствие лантаноидного сжатия), поэтому их свойства более сходны между собой, чем с марганцем. [31]
Вследствие лантаноидного сжатия атомные и ионные радиусы технеция и рения практически равны, поэтому их свойства в значительной степени сходны между собой. [32]
Как видим, атомные и ионные радиусы технеция и рения близки ( следствие лантаноидного сжатия), поэтому их свойства более сходны между собой, чем с марганцем. [33]
Современное состояние проблемы атомных и ионных радиусов в геохимии и кристаллохимии критически освещены в работах В. И. Лебедева, а также в исследованиях Дж. [34]
Чем обусловлена близость атомных и ионных радиусов молибдена и вольфрама. Как она сказывается на характере изменения свойств в ряду хром-вольфрам. [35]
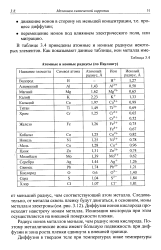 |
Атомные и ионные радиусы ( по Паулингу. [36] |
В таблице 3.4 приведены атомные и ионные радиусы некоторых элементов. [37]
Гафний и цирконий имеют почти одинаковые атомные и ионные радиусы. Они также весьма близки по химическим свойствам, как и следует ожидать, учитывая подобие их электронных конфигураций. В ионе гафния 4 / - электроны лежат слишком глубоко, чтобы оказывать заметное влияние на химические свойства. [38]
В табл. 76 сопоставлены атомные и ионные радиусы элементов четвертой главной подгруппы, рассчитанные по данным для кристаллических соединений. [39]
Для переходных элементов изменение атомных и ионных радиусов происходит не так просто, как у типичных элементов. Если рассмотреть изменение радиусов ряда переходных металлов по горизонтали ( табл. 4 - 2 и табл. 4 - 5), то можно увидеть, что происходит уменьшение и атомного, и ионного радиусов. Однако это уменьше ние неоднообразно и мало по сравнению с уменьшением, наблю даемьш в том же периоде для типичных элементов. Причина этого несомненно в том, что у переходных элементов прибавляющиеся электроны входят во внутренний ( п - 1) - слой. Эти электроны хорошо экранируют заряд ядра от ns - электронов, и размер атома остается почти постоянным. [40]
Для переходных элементов изменение атомных и ионных радиусов происходит не так просто, как у типичных элементов. Если рассмотреть изменение радиусов ряда переходных металлов по горизонтали ( табл. 4 - 2 и табл. 4 - 5), то можно увидеть, что происходит уменьшение и атомного, и ионного радиусов. Однако это уменьшение неоднообразно и мало по сравнению с уменьшением, наблюдаемым в том же периоде для типичных элементов. Причина этого, несомненно, в том, что у переходных элементов прибавляющиеся электроны входят во внутренний ( п - 1) й-слой. Эти электроны хорошо экранируют заряд ядра от ns - электронов, и размер атома остается почти постоянным. [41]
Для переходных элементов изменение атомных и ионных радиусов происходит не так просто, как у типичных элементов. Если рассмотреть изменение радиусов ряда переходных металлов по гори зонтали ( табл. 4 - 2 и табл. 4 - 5), то можно увидеть, что происходит уменьшение и атомного, и ионного радиусов. Однако это уменьшение неоднообразно и мало по сравнению с уменьшением, наблю даемым в том же периоде для типичных элементов. Причина этого несомненно в том, что у переходных элементов прибавляющиеся электроны входят во внутренний ( п - 1) с. Эти электроны хорошо экранируют заряд ядра от ns - электронов, и размер атома остается почти постоянным. [42]
Для переходных элементов изменение атомных и ионных радиусов происходит не так просто, как у типичных элементов. Если рассмотреть изменение радиусов ряда переходных металлов по горизонтали ( табл. 4 - 2 и табл. 4 - 5), то можно увидеть, что происходит уменьшение и атомного, и ионного радиусов. Однако это уменьшение неоднообразно и мало по сравнению с уменьшением, наблюдаемым в том же периоде для типичных элементов. Причина этого несомненно в том, что у переходных элементов прибавляющиеся электроны входят во внутренний ( п - 1) - слой. Эти электроны хорошо экранируют заряд ядра от ns - электронов, и размер атома остается почти постоянным. [43]
Общность свойств и близость атомных и ионных радиусов ниобия и тантала ( ионный радиус Nb 0 66, Та 0 66 А) обусловливают их совместное присутствие в природных минералах. [44]
Общность свойств и близость атомных и ионных радиусов ниобия и тантала обусловливает их совместное присутствие в природных минералах. [45]
Страницы: 1 2 3 4