Атомный ионный радиус
Cтраница 2
Атомные и ионные радиусы элементов главной подгруппы II группы значительно меньше радиусов соседних щелочных металлов. Это связано с большим зарядом и полным заполнением внешних электронных s - слоев щелочноземельных металлов. [16]
Поэтому атомные и ионные радиусы имеют определенные зависимости от порядкового номера в периодической таблице Менделеева и заряда иона. [17]
Имея почти одинаковые атомные и ионные радиусы вследствие лантаноидного сжатия ( Zr 0 145 нм; Ш 0 144 нм; Zr4 0 074 нм; Hf 0 075 нм), цирконий и гафний очень похожи друг на друга по химическим свойствам. Цирконий и гафний образуют всегда общие минералы. Наиболее удобными технологическими методами разделения циркония и гафния являются ионный обмен или жидкостная экстракция. [18]
 |
Радиусы главных максимумов плотности радиального распределения заряда электронов внешних орбиталей атомов. [19] |
Сумма атомных, ионных радиусов и радиусов, определенных по карте электронной плотности, соответствует экспериментально найденному межъядерному расстоянию только для КС1 и весьма приближенно для CuCl. В последнем случае более хорошим приближением является сумма атомных радиусов. [20]
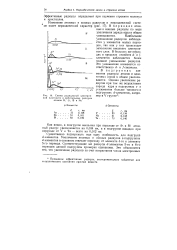 |
Схемы радиальной электронной плотности и орбитальные радиусы атомов Н, Li, В и Ne. [21] |
В периодах атомные и ионные радиусы по мере увеличения заряда ядра в общем уменьшаются. [22]
Как изменяются атомные и ионные радиусы с координационным числом. [23]
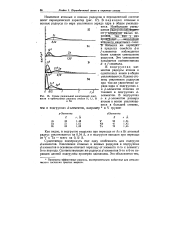 |
Схемы радиальной электронной плотности и орбитальные радиусы атомов Н, Li, В и Ne. [24] |
В периодах атомные и ионные радиусы по мере увеличения заряда ядра в общем уменьшаются. [25]
Наблюдаемая изменчивость атомных и ионных радиусов, в частности их зависимость при прочих равных условиях от координационных чисел, обусловлена взаимным влиянием соседних частиц. [26]
Близостью размеров атомных и ионных радиусов Тс и Re объясняется сходство их химических свойств. Химическая активность металлов в ряду Мп - Тс - Re понижается. [27]
Близостью размеров атомных и ионных радиусов Тс и Re объясняется сходство их химических свойств. Химическая активность металлов в ряду Мп-Тс - Re понижается. [28]
Большое сходство атомных и ионных радиусов РЗЭ находит отражение в значительном сходстве химических свойств этих элементов. [29]
Большое сходство атомных и ионных радиусов редкоземельных элементов находит свое отражение в значительном сходстве их химических свойств. Однако постепенное уменьшение радиусов при переходе от лантана к лютецию обусловливает я определенное химическое различие. [30]
Страницы: 1 2 3 4