Термохимический радиус
Cтраница 3
Наличие подобной простой зависимости между радиусом описанной сферы и термохимическим радиусом иона позволяет вычислить термохимические радиусы для серии других ионов с аналогичным строением ( В0 -, BeFf -, JC4, SeOf -, TeOf -, P04 -, AsC4 -, Sb04 -, BiC4 -), поскольку для них известны радиусы описанных сфер и форма. [31]
Выше мы указывали, что в результате расчета теплоты образования гексааквоманганоиодида, основанного на применении термохимических радиусов ионов, обнаружено серьезное расхождение между теоретически вычисленной величиной ( - ДЯ 298 491 ккал) и полученной Биховским и Россини [31] на основании опытных данных Лекера [84] по измерению упругости диссоциации данного гидрата. [32]
Энергия решетки солей с незначительной долей ковалентной связи определяется по уравнению Капустинского только зарядами и термохимическими радиусами ионов, образующих данную соль. Теплота гидратации ионов данного типа также однозначно определяется их зарядами и радиусами. Таким образом, и теплота растворения солей может быть выражена как функция двух переменных: радиуса катиона и радиуса аниона. [33]
Наряду с термохимическими величинами в таблицах приводятся радиусы ионов, вычисленные либо из термохимических данных ( термохимические радиусы), либо взятые из сводки Гольдшмидта. [34]
Из рассмотрения данных, приведенных в этой таблице, можно заключить, что по мере увеличения термохимического радиуса заместителя X в комплексном ионе [ Co ( NH3) 5X ] 2 растворимость соответствующих солей уменьшается. Из этого правила имеется несколько исключений, однако чаще всего эта закономерность наблюдается достаточно ясно. [35]
Приведенные в табл. 6 данные указывают на несомненно существующую связь между кристаллохимическпми характеристиками иона и его термохимическим радиусом. [36]
Исходя из данных по теплотам образования газообразных ионов, были рассчитаны энергии кристаллических решеток безводных силикатов кальция и термохимические радиусы ионов. [37]
Можно было предполагать, что в случае солей типа [ M ( NH3) 6 ] X2 и [ МЕп3 ] Х2 растворимость будет непрерывно уменьшаться от хлорида к иодиду, так как термохимические радиусы этих ионов в подавляющем большинстве случаев превышают 2 6 А. Поставленными нами опытами действительно удалось показать, что в случае гексамминникелевых солей и триэтилендиаминкадмиевых солей растворимость резко уменьшается от хлорида к иодиду. [38]
Воспользовавшись данными для теплоты образования [ Мп ( Н20) 4 ] 2 и теплотой образования [ Мп ( Н20) 4 ] С12, определенной нами совместно с Асташевой [85], мы нашли по методу Капустинского термохимический радиус [ Мп ( Н20) 4 ] 2 1; он оказался равным 1 61 А. [39]
В качестве объектов исследования нами были выбраны соединения различных типов: соединения щелочных металлов RbCNS, LiHC02 и LiCH3COO; щелочноземельных металлов Sr ( C103) 2; аквосоли [ Mg ( H20) e ] Br2, [ Ni ( H20) 6 ] ( G103) 2 и хлорат гексаммиаката никеля [ Ni ( NH3) e ] ( C103) 2, для которых были проверены значения теплот образования солей, вычисленных при помощи уравнения Капустинского, найденных нами термохимических радиусов и теплот образования газообразных ионов. [40]
Несимметричные ионы характеризуются так называемым термохимическим радиусом, который, по Капустин-скому, изоэнергетически замещает данный ион в кристаллической решетке. Термохимические радиусы ионов могут быть рассчитаны, например, методом разностей, предложенным Янимирским. [41]
Сама система термохимических радиусов содержит некоторые внутренние противоречия ( например, не увеличение, а уменьшение объемов по ряду ClOf - BrO - IO. Они могут поэтому играть лишь чисто расчетную роль. [42]
Как показали Капустинский и Яцимирский [62], термохимический радиус несферического иона не равен ни максимальному расстоянию от центра его до поверхности ( радиусу описанной сферы), ни минимальному расстоянию, а представляет собой некоторое среднее значение между этими двумя величинами. Так, например, термохимический радиус аниона 0 - равен 1 80 А; этот ион представляет собой эллипсоид вращения с полуосями, равными 1 98 и 1 24 А. [43]
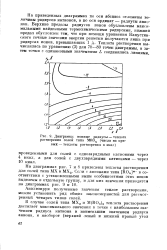 |
Диаграмма. ионные радиусы - теплота растворения солей типа MROn ( числа на кривых - теплоты растворения в ккал. [44] |
На приведенных диаграммах по оси абсцисс отложены величины радиусов катионов, а по оси ординат - радиусы анионов. Верхние пределы радиусов ионов обусловлены максимальными найденными термохимическими радиусами, нижний предел обусловлен тем, что при помощи уравнения Капустин-ского точные значения энергии решетки получаются лишь при радиусах ионов, превышающих 1 А. [45]
Страницы: 1 2 3 4