Орбитальный радиус
Cтраница 3
По сравнению с возбужденными состояниями легче производится расчет орбитальных радиусов ионов. Для катиона натрия, например, его орбитальный радиус определяется расстоянием от ядра до максимума электронной плотности 2р - электронов ( i-слой на рис. 21), так как у Na отсутствует 3 -электрон. Теоретический расчет орбитальных радиусов анионов аналогичен расчету соответствующих радиусов нормальных состояний. В табл. 7 приведены орбитальные и эффективные радиусы некоторых ионов и нейтральных атомов. [31]
По сравнению с возбужденными состояниями легче производится расчет орбитальных радиусов ионов. Для катиона натрия, например, его орбитальный радиус определяется расстоянием от ядра до максимума электронной плотности 2р - электронов ( L-слой на рис. 22), так как у Na отсутствует Ss-электрон. Теоретический расчет орбитальных радиусов анионов аналогичен расчету соответствующих радиусов нормальных состояний. В табл. 8 приведены орбитальные и эффективные радиусы некоторых ионов и нейтральных атомов. [32]
Если представим сферы с радиусами, равными по новым данным условным орбитальным радиусам нейтральных атомов для всей серии Q - LiF, то график, приведенный на рис. 104, показывает, как быстро растут атомные радиусы в ряду С, В, Be и Li и одновременно сжимаются в ряду С, N, О, F. В результате комбинация Li и F оказывается составленной из очень большой литиевой сферы и малой сферы фтора, при этом фтор более чем наполовину вдавлен в сферу лития. Если принять во внимание, что график составлен при помощи радиусов, отвечающих положению максимума радиальной плотности ( радиус средней радиальной плотности лежит примерно на 0 1 - 0 15 А дальше от ядра), внедрение атома фтора в сферу электронной оболочки атома лития будет почти полным. Известно, что ничтожный по величине голый протон внедряется в электронное облако молекулы аммиака, порождая NHt, но до появления новых значений атомных радиусов было трудно себе представить внедрение целого многоэлектронного атома фтора внутрь электронной сферы атома лития. [33]
 |
Вычисленные и экспериментально найденные значения длин связей ( в А. [34] |
Их называют атомными радиусами по Брэггу - Слейтеру и орбитальными радиусами, определяемыми по функции радиального распределения для внешних орбиталей атома. [35]
В последнее время достаточно широкое распространение получило представление об орбитальном радиусе, под которым понимается теоретически рассчитанное расстояние от ядра до главного максимума электронной плотности внешней орбитали. Радиус внешней орбитали атома или иона определяет атомный или ионный орбитальный радиус. [36]
 |
Зависимость значений электроотрицательности ЭО. [37] |
Ориентировочно можно считать, что элемент является неметаллом, если орбитальный радиус его атомов не превышает 0 1 нм. [38]
Причины двойной периодичности более подробно анализируются ниже при анализе изменения орбитальных радиусов и потенциалов ионизации с увеличением атомного номера. [39]
Внутренняя периодичность выражается в крутом наклоне линий, связывающих величины орбитальных радиусов s - элементов, более пологом - линий, связывающих р-элементы, и еще более пологом - d - и, наконец, / - элементы. Это объясняется увеличением числа электронов, находящихся в пределах одной подоболочки, при переходе от s - ( 2) к р - ( 6), d - ( 10) и / - элементам ( 14 электронов), при сохранении практически неизменным числа промежуточных электронов, экранирующих валентные электроны от ядра, и с достройкой у d - и / - элементов предвнепгаих электронных оболочек. [40]
У любого атома в невозбужденном состоянии может быть одно значение орбитального радиуса и множество значений для возбужденных состояний. Радиусы атомов имеют максимальное значение в начале периода, а затем несколько уменьшаются при переходе слева направо. Это связано с последовательным увеличением заряда ядра и, соответственно, числа электронов. При переходе к новому периоду радиус вновь резко увеличивается, так как при этом появляется новый энергетический уровень. [41]
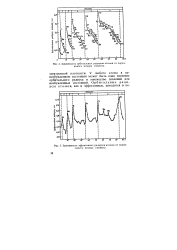 |
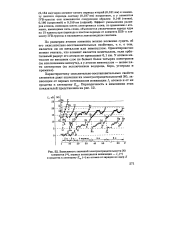
Зависимость орбитальных радиусов атомов от порядкового номера элемента.| Зависимость эффективных радиусов атомов от порядкового номера элемента. [42] |
У любого атома в невозбужденном состоянии может быть одно значение орбитального радиуса и множество значений для возбужденных состояний. [43]
Вторичная периодичность, вызванная второй из названных причин, выражается в нелинейном изменении орбитальных радиусов атомов с увеличением Z в пределах отдельных подгрупп Системы. Поэтому па рис. 3 г0рб Na лежит не на продолжении прямой Н - Li, а резко вправо от нее. [44]
В то же время эффективные радиусы катионов и анионов в несколько раз превосходят их орбитальные радиусы. [45]
Страницы: 1 2 3 4