Дигитонин
Cтраница 3
Исследуемую пробу экстрагируют смесью ацетона со спиртом и осаждают свободный холестерин дигитонином из части раствора. Общий холестерин осаждают точно так же из другой части раствора после щелочного гидролиза эфиров холестерина и определяют содержание холестерина в обоих осадках при помощи цветной реакции с уксусным. [31]
В зависимости от стереохи-мической конфигурации гидроксилов, мультислои некоторых стеролов специфически адсорбируют дигитонин. Мультислои хлорофилла не флуоресцируют, хотя отложенного количества хлорофилла было бы достаточно для заметной флуоресценции в растворе. [32]
К отфильтрованным жирным кислотам прибавляют 25 мл 1 % - ного раствора дигитонина в 96 % - ном спирте. Дигитонин, соединяясь со свободными стеринами, превращается в дегито-нид. Образующиеся кристаллы дигитонида отделяют от жирных кислот путем промывания на фильтре хлороформом и эфиром. Очищенный от жирных кислот дигитонид в продолжение 10 мин кипятят в 3 - 5 мл уксусного ангидрида. Реакционную смесь после охлаждения холодной водой обрабатывают четырехкратным количеством 50 % - ного спирта. Полученный при этом уксуснокислый стерин промывают на фильтре 50 % - ным спиртом, растворяют в небольшом количестве эфира и раствор выпаривают досуха в фарфоровой чашке. [33]
К отфильтрованным жирным кислотам прибавляют 25 мл 1 % - ного раствора дигитонина в 96 % - ном спирте. Дигитонин, соединяясь со свободными стеринами, превращается в дигито-нид. Образующиеся кристаллы дигитонида отделяют от жирных кислот путем промывания на фильтре хлороформом и эфиром. Очищенный от жирных кислот дигитонид в продолжении 10 мин кипятят с 3 - 5 мл уксусного ангидрида. Реакционную смесь после охлаждения холодной водой обрабатывают четырехкратным количеством 50 % - ного спирта. Полученный при этом уксуснокислый стерин промывают на фильтре 50 % - ным спиртом, растворяют в небольшом количестве эфира и раствор вы паривают досуха в фарфоровой чашке. После многократной кристаллизации определяют точку плавления. Температура плавления вещества выше 117 С указывает на идентичность его фитостерииу, что может служить доказательством присутствия в испытуемом жире растительного масла. Различные стерины имеют заметно отличную кристаллическую структуру. Поэтому бывает полезно выделить из полученных выше ацетатов стерины в чистом виде и просмотреть их под микроскопом. На основании микроскопического исследования также можно судить о происхождении жира, из которого были получены стерины. [34]
В отличие от эргостерина ни один из его продуктов облучения не осаждается дигитонином, а из продуктов пиролиза осаждается частично лишь изопирокальциферол. Двойная связь эргостерина, находящаяся в положении 22 23, не принимает участия в рассмотренных превращениях, так как все первые пять изомергых продуктов дают в результате озонирования метилизопропилацетальдегид-130. Степень ненасыщенности различных продуктов превращений была установлена путем микрогидрирования или при помощи титрования надбензойной кислотой. Число колец, определенное по степени ненасыщешюсти соответствующих соединений и на основании аналитических данных, подтверждено результатами опытов по дегидрированию этих соединений. Было установлено, что в молекуле лумистерина, так же как и в молекуле эргостерина, имеются три двойные связи и, следовательно, четыре кольца и что в результате дегидрирования селенрм из лумистерина получается углеводород Дильса; следовательно, это вещество является стереоизомером эргостерина. [35]
Все три продукта являются изомерами эргостерола и не обладают антирахитической способностью; дигитонином они не осаждаются. Супрастеролы являются конечными продуктами фотохимической реакции. Они содержат четыре кольца, боковую цепь и гидроксильную группу, подобно эргостеролу. [36]
Спиртовой раствор нагревают почти до кипения, добавляя к нему по каплям раствор дигитонина. Для полного осаждения стеринов добавляют в 6 - 8 раз больше дигитонина, чем требуется по уравнению реакции. Стерины отфильтровывают, а фильтрат разбавляют вдвое водой и экстрагируют в делительной воронке тремя порциями по 25 мл эфира. [37]
О структуре люмисте-рина позволяют судить следующие факты: он не образует осадка с дигитонином ( см. сноску б в табл. 30 - 2), хотя эпилюмистерин ( см. упражнение 30 - 23) дает такой осадок; полностью гидрированный люмистерин не идентичен ни полностью гидрированному эргосте-рину, ни полностью гидрированному эпиэргостерину; люмистерин при дегидрировании образует циклопентанофенантрен ( стр. [38]
О структуре люмистерина позволяют судить следующие факты: он не образует осадка с дигитонином ( см. сноскуб в табл. 30 - 2), хотя эпи-люмистерин ( см. упражнение 30 - 23) дает такой осадок; полностью гидрированный люмистерин не идентичен ни полностью гидрированному эргостерину, ни полностью гидрированному эпиэргостерину; люмистерин при дегидрировании образует циклопентанофенантрен ( гл. [39]
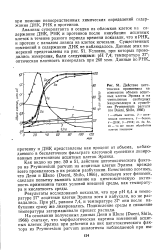 |
Действие цита-токсина примнезина на изменение объема асцитных клеток Эрлиха и на уменьшение свободных макромолекул в суспензии Prymnesium parvunt ( по Daeni, Shilo, 1966. [40] |
ДНК представлены как процент от объема, наблюдаемого в бесклеточном фильтрате клеточной суспензии лизиро-ванных дигитонином асцитных клеток Эрлиха. [41]
Из этих трех изомеров, обладающих несвойственной природным стеринам конфигурацией, осаждается ( частично) дигитонином один лишь изопирокальциферол, в котором 10-метильная группа обладает нормальной ориентацией. [42]
Молекулярный комплекс, получивший название дигитонида холестерина, состоит из одной молекулы холестерина и одной молекулы дигитонина. Дигитонид не имеет определенной точки плавления, но выделяется из растворов в виде характерных кристаллов. Растворимость этого вещества настолько незначительна ( 0 014 г в 100 мл 95 / 0-ного спирта при 18), что оно может быть легко очищено от посторонних примесей. В спиртовых растворах происходит диссоциация комплекса на компоненты до определенной, хотя и слабой степени. Осаждение холестерина и других стеринов при помощи дигитонина применяется также при выделении стеринов из смесей. Для обратного выделения стеринов и очень дорогого дигитонина требуется применение специальных способов, так как эти молекулярные соединения настолько устойчивы, что не разлагаются, например, даже при продолжительной экстракции эфиром. При кипячении дигитонидов с ксилолом в продолжение нескольких часов стерины могут быть выделены обратно; однако некоторые стерины недостаточно устойчивы для подобной обработки. При этом стерин остается в растворе. Этот способ разложения представляет ценность для выделения таких соединений, как, например, Д4 - холестенол, который легко теряет молекулу воды. [43]
Для весового определения холестерина используют труднорастворимый комплекс ( дигитонид), образуемый им со стероидным сапонином дигитонином ( стр. [44]
Для весового определения холестерина используют труднорастворимый комплекс ( дититоиид), образуемый им со стероидным сапонином дигитонином ( стр. [45]
Страницы: 1 2 3 4