Дигликоль
Cтраница 3
Внедрение отдельного звена ( 3) в цепь в инвертированном структурном положении дает возможность наблюдать образование различных изомеров дигликоля. Озонирование приводит к образованию сложных эфиров, кетонов, альдегидов и соединений с карбоксильными группами, которые восстанавливаются до спиртов алюмогидридом лития. Вероятно, что многие вторичные спирты образуются при восстановлении кетонов и таким образом происходит потеря их первоначальной конфигурации. [31]
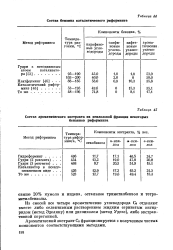 |
Состав бензина каталитического риформинга. [32] |
Из смесей все четыре ароматические углеводорода Се отделяют вместе либо селективным растворением жидким сернистым ангидридом ( метод Эделяну) или дигликолем ( метод Удекс), либо экстрактивной перегонкой. [33]
Как только температура в верхней части дефлегматора опустится ниже 100 С, систему откачивают до 12 - 14 мм рт. ст, На этой стадии следует обратить внимание на возможность переброса дигликоля и по мере необходимости откачивать более медленно. Поддерживая постоянными температуру ( 200 С) и давление реакционной смеси ( 12 - 14 мм рт. ст.), через каждые 5 ч отбирают пробу для определения кислотного числа. Для отбора пробы систему заполняют азотом, а затем снова откачивают. После охлаждения в атмосфере азота слаборазветвленный полиэфир представляет собой вязкую, светло-желтую массу. [34]
С карболовыми кислотами получают сложные эфиры гликолей. Эфир дигликоля и бензойной кислоты представляет собой неядовитый пластификатор для поливинилхлорида. [35]
С карбоновыми кислотами получают сложные эфиры гликолей. Эфир дигликоля и бензойной кислоты представляет собой неядовитый пластификатор для поливинилхлорида. [36]
Моноэфиры, полученные этерификацией трихлоруксусной кислоты гликолем или дигликолем, растворяют применяемый в производстве волокна триацетат при комнатной температуре. Вместо дигликоля можно для этерификации применять тиодигликоль S ( СН2СН2ОН) 2, но удлинение углеродной цепи гликоля на 4 атома углерода, по-видимому, значительно ослабляет сольватирующую способность моноэфира. Поэтому бутиленгли-колевый или тиодибутиленгликолевый моноэфиры уже не являются растворяющими пластификаторами. Он хорошо совмещается с ацетатом целлюлозы в пленке и оказывает длительное эффективное действие. [37]
Теплота сгорания дигликоля равна 566 Кал на моль. При обыкновенной температуре дигликоль легко смешивается с водой, низшими спиртами, этиленгликолем, ледяной уксусной кислотой, ацетоном, фурфуролом, пиридином, гликольдиацетатом, хлороформом, нитробензолом и анилином. Дигликоль не растворяется в эфире, бензоле, толуоле, сероуглероде и че-тыреххлористом углероде. Это соединение - хороший растворитель для нитроцеллюлозы и различных красителей; оно не растворяет эфирных смол, шеллака, кумароновых смол, копалов и ацетилцеллюлозы. При хранении над водой в закрытой посуде дигликоль абсорбирует ее в течение 9 дней больше своего собственного веса, но при этом совершенно не претерпевает гидролиза. [38]
Лаковые смолы получают также этерификацией канифоли. Этерификацию канифоли, например глицерином или дигликолем, следует вести при высокой температуре. Больше половины вырабатываемой канифоли расходуется на проклейку бумаги. [39]
Гликоли при межмолекулярном выделении воды могут ступенчато превращаться в полигликоли. Обычный этиленгликоль под действием водоотнимающих средств при нагревании образует сперва дигликоль, но процесс может идти и дальше, в результате получаются полигликоли различной сложности-от вязких жидкостей до твердых веществ. [40]
К настоящему времени разработаны способы получения ряда новых видов синтетических каучукоподобных материалов, которые еще не нашли широкого промышленного применения. К таким полимерам относятся полиакриловые каучуки, полиуретано-вые каучуки-продукты взаимодействия дигликолей с дикарбо-новыми кислотами с последующей обработкой диизоцианатами, хлорсульфированный полиэтилен и некоторые другие. Особенное внимание уделяется разработке способов получения и изучению свойств фтор содержащих каучукоподобных полимеров, в частности на основе сополимеризации трифторхлорэтилена с другими непредельными соединениями. [41]
Как в некаталитических реакциях, так и при использовании кислотных и основных катализаторов наиболее важным фактором, влияющим на выход оксиалкилированных продуктов, является соотношение спирт: окись. Даже при 8 - 10-кратном избытке спирта наряду с эфиром моногликоля образуется эфир дигликоля. Если учесть, что в настоящее время все эфиры полигликолей находят широкое применение, выбор способа синтеза будет определяться не столько образованием этих полиэфиров, сколько скоростью реакции и наличием посторонних ( альдегиды, 1 4-диоксан, диэфири) примесей. В этом смысле предпочтение отдается нейтральному и слабощелочному синтезам. [42]
Замещением гидроксильной группы гликолевой кислоты группой простого эфира и этерификацией ее спиртом с достаточно длинным радикалом можно получить вещества, удовлетворяющие требованиям, предъявляемым к пластификаторам. Фирма Monsanto Chemical4 предложила применять в качестве пластификатора феноксиуксусную кислоту, карбоксильная группа которой этерифицирована дигликолем. [43]
Дигликольстеарат ( гликостерин) - белое воскоподобное вещество с легким запахом жира, нейтральной реакции, плавится при 54 С и полностью диспергируется в горячей воде. В химическом отношении - это неполный сложный эфир стеариновой и пальмитиновой кислот и моно - и дигликоля. Многие из существующих в продаже сортов не содержат щелочей или аминов, однако лучшие эмульгаторы получаются при предварительной обработке его едким кали или натром. [44]
Особенно подходят вещества с большим числом свободных электронных пар в молекуле, такие как монометиловый эфир гликоля, монометиловый эфир дигликоля и монометиловый эфир полиэтилен-гликоля. [45]
Страницы: 1 2 3 4