Величина - термодинамический потенциал
Cтраница 1
Величина термодинамических потенциалов изменяется также вследствие изменения масс реагирующих веществ, входящих в состав физико-химической системы. Для системы, состоящей из нескольких составных частей, которые могут вступать в химическое взаимодействие, термодинамический потенциал является функцией не только состояния, но и состава системы. [1]
Величина термодинамического потенциала плазмы определяется в данном случае суммой величин ( II. [2]
Величины термодинамических потенциалов реакций восстановления окислов гидридом натрия рассчитывали для стандартных условий и температуры 650 К, при которой обычно ведут обработку металлов в гидридном расплаве. [3]
Зная величины термодинамических потенциалов и энтропии, можно через них и их производные определить все термодинамические свойства системы. [4]
Для определения величины термодинамического потенциала (7.38) необходимо знать величины энтропии и температуры, так как величина разности энтальпий нами была рассчитана при рассмотрении первого начала термодинамики. [5]
Таким образом, величина термодинамического потенциала показывает устойчивость или неустойчивость данной системы и соответственно направление самопроизвольного процесса. [6]
Эти же условия определяют и величину термодинамического потенциала и его изменение в результате достижения, обратимого химического равновесия. [7]
Интенсивность электромолекулярного взаимодействия фаз в коллоидном растворе характеризуется величиной термодинамического потенциала, которая зависит от общего числа адсорбированных частиц ионов. [8]
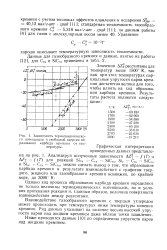 |
Зависимость термодинамическо. [9] |
Однако ход процесса образования карбида кремния определяют не только величины термодинамических потенциалов, но и условия протекания реакции и, главным образом, величина поверхности взаимодействия между реагентами. [10]
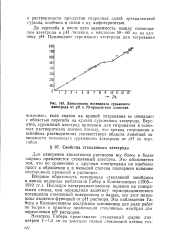 |
Зависимость потенциала сурьмяного электрода от рН в 70-процентном алкоголе. [11] |
Исследуя электрокинетические явления на поверхности стекла, они определили величину термодинамического потенциала стеклянной поверхности и нашли, что этот потенциал является функцией от рН раствора. Эти наблюдения Га-бера и Климансиевича послужили основанием для ряда работ по теории и практике применения стеклянных мембран для определения рН растворов. [12]
Исследуя электрокинетические явления на поверхности стекла, они определили величину термодинамического потенциала стеклянной поверхности и нашли, что этот потенциал является функцией рН раствора. Эти наблюдения Габера и Кли-мансиевича послужили основанием для ряда работ по теории и практике применения стеклянных мембран для определения рН растворов. [13]
Исследуя электрокинетические явления на поверхности стекла, они определили величину термодинамического потенциала стеклянной поверхности и нашли, что этот потенциал является функцией рН раствора. Эти наблюдения Габера и Климансиевича послужили основанием для ряда работ по теории и практике применения стеклянных мембран для определения рН растворов. [14]
В качестве иллюстрации применим уравнение ( 50) для вычисления величин термодинамического потенциала для НС1, НВг и HJ в интервале 300 - 2000 К. [15]
Страницы: 1 2 3