Величина - равновесный потенциал
Cтраница 1
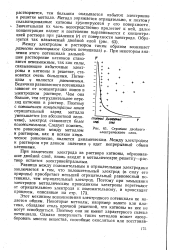 |
Строение двойного электрического слоя. [1] |
Величина равновесного потенциала зависит от концентрации ионов в электродном растворе. [2]
Определение величины равновесного потенциала стали приобретает исключительный интерес для окончательного решения рассматриваемого вопроса. Методически непосредственное определение равновесного потенциала: может быть выполнено для электродов, образующих на поверхности защищаемого металла гидроокис-но-карбонатные осадки, путем анализа кривых после отключения тока поляризации. [3]
Так, величина равновесного потенциала не зависит от природы металла индифферентного электрода ( Pt, Ir, Au, Rh и другие), величина же стационарного потенциала зависит. [4]
Так как величина равновесного потенциала электрода определяется изменением термодинамического потенциала в ходе электродной реакции и не должна зависеть от структуры двойного электрического слоя, наибольший интерес представляет рассмотрение того частного случая, когда система достаточно далека от состояния равновесия. [5]
Нормальные потенциалы; Прямое измерение величины равновесного потенциала неосуществимо. Для получения цифровых данных используется косвенный путь, основанный на определении величины потенциала одного электрода относительно величины потенциала другого электрода. [6]
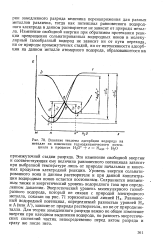 |
Влияние теплоты адсорбции водорода на металле на изменение термодинамического потенциала в процессе Н3О е Надс Н2О. [7] |
Это изменение свободной энергии1 и соответствующая ему величина равновесного потенциала зависят при выбранной температуре лишь от природы начальных и конечных продуктов электродной реакции. Уровень энергии сольвати-рованного иона в данном растворителе и при данной концентрации водородных ионов остается постоянным. Сохраняется неизменным также и энергетический уровень водородного газа при определенном давлении. Равновесный водородный потенциал, определяемый разностью уровней Н2 и А ( или А), зависит от природы растворителя, но не от природы металла. Для теории замедленного разряда важно не общее изменение энергии при катодном выделении водорода, но разность энергетических состояний частиц непосредственно перед актом разряда и сразу же после него. [8]
 |
Исходные данные к контрольному примеру. [9] |
Известно, что в том же растворе величины равновесных потенциалов алюминия, никеля, титана и железа составляют соответственно: - 1 7; - 0 42; - 1 62; - 0 46 В. Установить, для каких из указанных металлов цинк может обеспечить протекторную защиту, и рассчитать для этих металлов, как и для цинка, величину водородного перенапряжения при плотности тока, равной к. [10]
Это изменение свободной энергии ( и соответствующая ему величина равновесного потенциала) зависит при выбранной температуре от природы начальных и конечных продуктов электродной реакции. Уровень энергии сольватированного иона в данном растворителе и при данной концентрации водородных ионов остается постоянным. Сохраняется неизменным также и энергетический уровень водородного газа при определенном давлении. Равновесный водородный потенциал, определяемый разностью уровней Н2 и А ( или А), зависит от природы растворителя, но не от природы металла. Для теории замедленного разряда важно не общее изменение энергии при катодном выделении водорода, а разность энергетических состояний частиц непосредственно перед актом разряда и сразу же после него. [11]
Тем не менее, электрохимические исследования, пытающиеся связать величины равновесных потенциалов и поляризационные характеристики с определенными кристаллографическими направлениями, являются очень важными и заслуживают большого внимания. Особенно важен этот вопрос для интерпретации коррозии сплавов. [12]
Фа радея, k - коэффициент, зависящий от величины равновесного потенциала железа. [13]
Из формулы ( 7) следует, что для определения величины равновесного потенциала компонента сплава, образующего твердый раствор или интерметаллическое соединение, необходимо знать изменение парциальной молярной свободной энергии металла при переходе его из состояния чистого металла в сплав. [14]
Для многих окислительно-восстановительных реакций ( особенно с участием сложных органических соединений) величину равновесного потенциала непосредственно измерить невозможно. В отличие от потенциала кислородного электрода ее не всегда удается и рассчитать. Поэтому для характеристики кинетики окислительно-восстановительных реакций часто используют не величину поляризации, а непосредственное значение электродного потенциала под током. [15]
Страницы: 1 2 3 4