Величина - атомный радиус
Cтраница 2
 |
Атомные и ионные радиусы химических элементов. [16] |
Периодическая система элементов позволяет установить закономерности в изменениях величин атомных радиусов, ионных радиусов и потенциалов ионизации. Величины атомных и ионных радиусов закономерно увеличиваются в группах элементов в направлении сверху вниз. С увеличением порядкового номера элемента внутри периода атомные и ионные радиусы уменьшаются по горизонтали слева направо к середине периода, а затем вновь увеличиваются. [17]
 |
Зависимость между изменением процента d - характера ряда металлов и логарифмом их активности, отнесенной к единице площади поверхности, для реакции. [18] |
Но следует помнить, что б контролирует только величину атомного радиуса или межатомные расстояния в решетке; на основании данных о 8 нельзя получить точное представление о расположении активных центров на данной поверхности. [19]
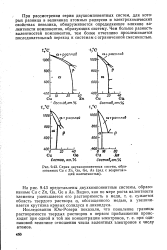 |
Серия двухкомпонентных систем, образованных Си с Zn, Ga, Ge, As ( ряд с возрастающей валентностью. [20] |
При рассмотрении серии двухкомпонентных систем, для которых разница в величинах атомных радиусов и электрохимических свойствах невелика, обнаруживается определяющее влияние валентности компонентов, образующих систему. Чем больше разность валентностей компонентов, тем более отчетливо прослеживается последовательный переход к системам с ограниченной смесимостью. [21]
Если структура металла характеризуется иными координационными числами, то для получения величины атомного радиуса недостаточно знания половины кратчайшего межатомного расстояния. В это значение должна быть внесена поправка на координационное число. Величины поправок были указаны в табл. 16 на стр. [22]
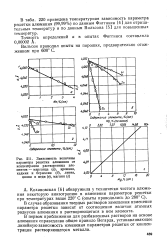 |
Зависимость величины параметра решетки алюминия от концентрации растворенных элементов - марганца ( а, кремния, кадмия и бериллия ( б, лития, цинка и меди ( в, магния ( г. [23] |
В случае образования твердых растворов замещения изменение параметра решетки зависит от соотношения величин атомных радиусов алюминия и растворяющегося в нем элемента. [24]
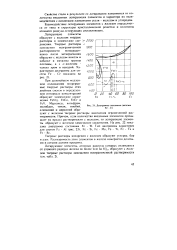 |
Диаграмма состояния системы Fe - Cr. [25] |
Взаимодействие легирующих элементов с железом определяется от типа и структуры кристаллической решетки и величины атомного радиуса легирующих составляющих. [26]
Кр и Ри, наиб, близкими к II по электронной структуре и величине атомных радиусов, образуется непрерывный ряд твердых р-ров на основе у-фазы II, а также широкие области твердых р-ров на основе Р - ( до 26 ат. [27]
Связаны ли и всегда ли связаны границы образования твердых растворов замещения с различиями в величине атомных радиусов растворителя и растворенного. Насколько такой подход оправдан. [28]
 |
Температурно-временные зависимости. [29] |
Металлы, значительно отличающиеся порядковым номером от титана, очень разные по электронному строению и величине атомных радиусов, плохо свариваются с титаном. Между тем во многих отраслях техники оптимальные служебные свойства сварных изделий можно получить при изготовлении их в сочетании титана именно с этими металлами. [30]
Страницы: 1 2 3 4