Величина - атомный радиус
Cтраница 4
Какие радиусы отвечают по смыслу понятию атомный радиус. Поясните, как влияют на величину атомного радиуса следующие факторы: эффективный заряд ядра, конфигурация внешнего электронного слоя, число электронных слоев, тип химической связи и ее кратность. [46]
Может показаться, что наиболее благоприятные условия для образования водородной связи ( наибольшее сближение хлора и ОН-группы) должны быть вф - кокформации зтиленхлсргидрина. Однако рассмотрение геометрии молекулы с учетом величины атомных радиусов показывает, что это не так. Дело в том, что любые заместители ( кроме водорода и фтора), стоящие при соседних атомах углерода, при расположении в четной ф - кон-формации слишком сближены, расстояние между нимк оказывается меньшим, чем сумма их радиусов действия. Поэтомх четные конформации, как правило, неустойчивы. [47]
АВ) - образуются обычно при определенном соотношении атомных радиусов компонентов гд / / - в и обладают узкими областями гомогенности. Ша, ГУа, Нб-Уб при условии достаточно малого различия в величинах атомных радиусов компонентов образуются фазы Юм-Розери, часто наз. Фазы образуют переходные металлы гл. [49]
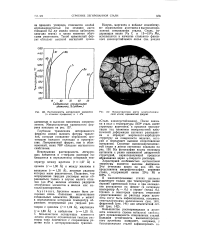 |
Растворимость легирующих элементов ( в атомных процентах в - Fe. [50] |
А), атомные радиусы которых мало различаются. Полагают, что непрерывные твердые растворы могут образоваться только в случае малого отличия ( до 8 / о) величин атомных радиусов легирующих элементов и железа как металла-растворителя. [51]
Следовательно, легко видеть, почему осмий и рутений, с их гексагональной плотноупакованной кристаллической решеткой, не показывают полной смешиваемости с платиной или палладием. Однако имеющиеся данные свидетельствуют об умеренной растворимости рутения в этих двух металлах, чего и следовало ожидать, судя по величине атомных радиусов и по валентности этих элементов. Полная растворимость железа в платине или палладии хорошо увязывается с фактом повышения температуры, у - р-перехода при введении небольшой добавки этих металлов. Сплавы, содержащие менее 5 % платины, кристаллизуются в кубической гранецен-трированной решетке. Теория не дает объяснения, почему родий и иридий вообще не растворяются в серебре. [52]
Весьма удачно с помощью этой теории могут быть объяснены люминесцентные свойства нежестких молекул. Для суждения о том, возможна или нет люминесценция такого-то рода молекул, Божевольнов предлагает строить силовую модель молекулы, используя данные по величинам атомных радиусов, длине связей и величине валентных углов. Построенная таким образом модель позволяет судить о том, является ли данная молекула копланар-ной или некопланарной и имеются ли у нее зоны перекрывания. Если модель молекулы позволяет установить отсутствие зон перекрывания, то можно утверждать, что при выполнении ряда других условий такая молекула способна флуоресцировать. В том случае, когда имеются зоны перекрывания силовых полей отдельных частей молекулы и переход из одного конформационного изомера в другой связан с преодолением взаимодействия этих зон, то вероятность люминесценции уменьшается, так как на преодоление подобного рода пространственных затруднений затрачивается часть энергии возбуждения. [53]
У скандия очередной электрон поступает не во внешнюю, а в предыдущую Зе. Заполнение 3d - оболочки оказывает определенное экранирующее действие, ослабляющее притяжение ядром внешней оболочки. Поэтому уменьшение величин атомных радиусов у З - элементов выражено менее резко, чем при переходе от калия к кальцию. У меди и цинка наблюдается даже некоторое увеличение атомных радиусов. По-видимому, здесь проявляется влияние заполненного Зй-уровня, что выражается в увеличении его экранирующего эффекта. [54]
В действительности вообще выделение этих фаз в самостоятельную группу фаз внедрения недостаточно оправдывается ни по условиям их образования, ни по их основным свойствам. Об этом свидетельствуют также отмеченные исключения для монокарбидов вольфрама и молибдена и некоторых нитридов. Кроме того, величина атомного радиуса углерода или азота в соответственных соединениях ( эффективный радиус) может значительно отличаться от его исходной величины. [55]
Такой тройной контроль, естественно, исключает возможность существования некоторых соединений в виде природных минералов. Это явление хорошо иллюстрируется полевыми шпатами - алюмосиликатами калия, натрия и кальция. Уже по величине валентности можно ожидать, что другие щелочные металлы способны замещаться литием, однако благодаря значительной разнице в величинах атомных радиусов такое замещение невозможно. С другой стороны, рубидий и барий могут замещать калий, в то время как магний и железо ( II) неспособны замещать кальций. Другими словами, при образовании кристаллических минералов доминирующее значение имеет величина ионов, а их валентность и сочетания энергии играют меньшую роль. Это положение особенно справедливо для силикатов. Кроме того, так как геометрические факторы до такой степени преобладают в минерализации, принцип изоморфизма приобретает большее значение для геохимика, чем для химика, задачей которого является приготовление чистых химических соединений в лаборатории. [56]
Для оценки люминесцентной активности вещества Е. А. Бо-жевольнов предложил использовать представления о конфор-мационной изомерии, основываясь на теории тушения люминесценции за счет потери молекулой поглощенной энергии при относительных поворотах ее отдельных частей, а также используя данные об оптических изменениях в молекуле при / 4 с-гранс-изомеризации, наблюдающейся при действии ультрафиолетового света. Весьма удачно с помощью этой теории могут быть объяснены люминесцентные свойства нежестких молекул. Для того чтобы узнать, возможна ли люминесценция молекулы, Божевольнов предлагает построить ее силовую модель, применив данные о величинах атомных радиусов, длине связей и величине валентных углов. [57]
Во многих случаях приложения термического анализа достаточно определить температуру остановок и указать их относительные величины в серии сплавов. Однако для определения природы превращения бывает необходимо более детальное знание термических эффектов. Примером является превращение порядок - беспорядок, происходящее при высокой температуре, которое не может быть обнаружено обычными рентгеновскими методами вследствие того, что изменение структуры произошло уже при низких температурах или из-за очень малого различия в величине атомных радиусов компонентов сплава. Качественные методы, описанные в главе И, полезны, но доказательство является более убедительным, если для области превращения установлено соотношение между удельной теплоемкостью и температурой. В принципе термический анализ может быть использован для измерения скрытой теплоты и теплоемкости, но на практике очень трудно получить количественные данные из кривых охлаждения, снятых обычным путем. [58]
Страницы: 1 2 3 4
