Величина - степень - диссоциация
Cтраница 3
Приближенным графическим решением уравнения ( 7) и были найдены величины степеней диссоциации окиси лития. [31]
Состав равновесной смеси и температура сгорания могут быть определены либо с помощью величин степеней диссоциации всех реакций диссоциации, либо непосредственно на основе использования закона сохранения массы элементов. [32]
 |
Константы диссоциации некоторых двухосновных кис. о. при 25 С. [33] |
Аррениус предполагал, что все электролиты лишь частично диссоциированы в растворах любых концентраций и отличаются друг от друга величиной степени диссоциации. Это неверное положение было общепринято до 20 - х годов текущего столетия. [34]
В / см) можно прочесть так: ионы движутся со скоростями, не зависящими от концентрации С, но концентрация определяет величину степени диссоциации а; поэтому при возрастании С ( когда уменьшается а) наблюдается уменьшение К. [35]
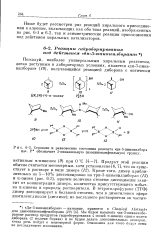 |
Строение и равновесные состояния реагента ди-3 - пинанилбора на. Р обозначает 3-пинанильную ( изопинокамфеипьную группу. [36] |
Кроме того, димер приблизительно на 5 - 10 % диссоциирован на три-3 - пинанилдиборан ( 13) и а-пипен ( рис. 6 - 3), причем величина степени диссоциации зависит от концентрации димера, количества присутствующего избытка ос-пинена и природы растворителя. [37]
Сильные электролиты даже в разбавленных растворах не ведут себя как растворы идеальные. Величина степени диссоциации таких электролитов, определенная различными способами, оказывается различной, при этом расхождения в данных больше, чем это могло бы быть вызвано погрешностями опыта. Для сильных электролитов степень диссоциации представляет кажущуюся величину. [38]
Электролиты подразделяются на слабые и сильные. Количественно ионизация электролита характеризуется величиной степени диссоциации ( а), которая равна отношению числа диссоциированных молекул к общему числу растворенных молекул. Сильные электролиты в растворах практически состоят только из ионов. [39]
Для уксусной кислоты степень диссоциации в этом выражении равна одному проценту. Очевидно, что в таком выражении величины степени диссоциации будут в 100 раз больше, чем при выражении степени диссоциации в долях грамм-молекулы. [40]
Введем в качестве меры электролитической диссоциации величину степени диссоциации а, определяемую как долю молекул, распавшихся на ионы ( сравн. [41]
Теория Дебая и Гюккеля поэтому иногда называется Теорией полной диссоциации. Действительно, определив из интенсивности светопогло-щения величину степени диссоциации раствора слабого электролита, можно найти истинную концентрацию его ионов, а затем по уравнению ( 126) и средний коэффициент активности. [42]
Чем больше ДИСс, тем сильнее диссоциирован слабый электро-лит. Наряду с / Сдисс для количественной характеристики равновесия используют величину степени диссоциации а. Она характеризует долю молекул слабого электролита, которые диссоциировали в растворе на ионы. Степень диссоциации связана с константой диссоциации. Взаимосвязь между ними может быть найдена следующим образом. Если начальная концентрация растворенного слабого электролита равна С молей в 1 л, то после диссоциации в состоянии равновесия [ А ] аС; [ Х - ] аС; [ АХ ] ( 1 - а) С. [43]
Способность растворов электролитов проводить электрический ток зависит от подвижности ионов. Изучение этого явления позволяет получить информацию о многих важных свойствах раствора ( о величинах степени диссоциации и константы диссоциации слабых электролитов, активности и коэффициента активности сильных электролитов) и определить изотонический коэффициент. Различия в подвижностях ионов используются для контроля за протеканием различных процессов. [44]
Страницы: 1 2 3