Величина - теплота - адсорбция
Cтраница 3
Далее, если допустить, что величины теплот адсорбции в зависимости от доли заполненной поверхности могут быть удовлетворительно объяснены взаимодействием адсорбированных атомов, то становится очевидным, что на поверхности должно быть ограниченное число атомов, достаточно удаленных друг от друга для того, чтобы взаимодействия между ними не было. Допустив, что каждое положение представляет квадрат и что все соседние положения являются объектами взаимодействия, мы увидим, что заполнения долей поверхности порядка одной девятой ее величины и менее должны дать независимость теплоты адсорбции по степени заполнения. Франкенбурговская величина 0 8 % заполнения, ниже которой теплота адсорбции становится постоянной, превышается на 3 2 % при учете того, что фактически только одна четверть исследовавшейся им поверхности была свободной. Так как величина 3 2 не совпадает с ожидаемой величиной 11 %, мы не должны забывать, что три четверти поверхности покрыты окисью кремния, которая может неизвестным образом ( распределение двуокиси кремния неизвестно) влиять на понижение этого процента ( 11 %), если допустить, что взаимодействие водорода с окисью кремния, по соседству с которой он адсорбирован, приблизительно того же порядка, что и взаимодействие между двумя адсорбированными рядом друг с другом атомами водорода. [31]
Графом [33] было замечено, что величины теплот адсорбции многих веществ, в том числе азота, кислорода, окиси углерода и метана, определяются природой катиона, входящего в состав цеолита. Адсорбционное взаимодействие в сильной мере зависит от природы катиона цеолита и может определить инверсию порядка вымывания отдельных компонентов в процессе их разделения. [32]
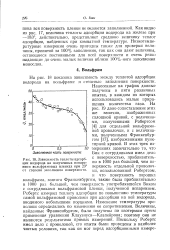 |
Зависимость теплоты адсорбции водорода на полученных испарением вольфрамовых пленках при 23 от степени заполнения поверхности. [33] |
Как видно из рис. 17, величина теплоты адсорбции водорода на железе при - 183, действительно, представляет среднюю величину теплот адсорбции, найденных при комнатной температуре. Низкотемпературные измерения очень пригодны также для проверки величины, принятой за 100 % заполнения, так как они дают величины, остающиеся постоянными для всей поверхности и очень резко падающие до очень малых величин вблизи 100 % - ного заполнения монослоя. [34]
Было бы очень полезно сравнить также величины теплот адсорбции водорода, определенные из адсорбционных измерений, с полученными из кинетических данных. Как можно видеть из табл. 2 и рис. 5 доклада 31, абсолютные величины адсорбционных коэффициентов водорода, полученные из кинетических и адсорбционных измерений, различны. [35]
Темкиным и автором [6] были оценены величины теплот адсорбции азота, оптимальные для реакции синтеза аммиака, идущего через лимитирующую стадию - адсорбцию азота: qom 38 ккал / молъ для 450 С и 1 атм и допт 30 3 ккал / молъ для 300 атм. Как известно, тантал не является катализатором синтеза аммиака, хотя хорошо адсорбирует азот. [36]
Следовательно, при постоянном энтропийном слагаемом величины теплот адсорбции каждого из поверхностных соединений при переходе от одного места к другому изменяются на одну и ту же величину. [37]
Для нормальных алканов наблюдается линейная зависимость величины теплот адсорбции от числа атомов углерода. Для фторуглеводородов с одинаковым числом атомов углерода теплоты адсорбции уменьшаются с ростом молекулярного веса. Для всех исследованных веществ теплоты адсорбции близки к теплотам конденсации. [38]
В табл. 8.18 - 8.23 приведены некоторые величины изостери-ческих теплот адсорбции и показано, как они изменяются с увеличением количества адсорбированного вещества. Для большинства цеолитов изостерические теплоты даны для двух катионных форм при малых, близких к нулевым, и высоких степенях заполнения адсорбатом. Приведенные данные позволяют судить о степени однородности внутренней поверхности по отношению к данному адсорбату. [39]
Применение указанной модели затруднено отсутствием в литературе величин теплот адсорбции нефтепродуктов на поверхностях сталей. [40]
Физическую и химическую адсорбцию можно различать по величине теплоты адсорбции - теплота физической адсорбции не выше 7 - 8 ккал / моль, а для хемосорбции характерна величина-15 - 17 ккал / молъ ( хемо-сорбцию можно характеризовать также величиной - 2 5 - 3 0 мк молъ / м, а физическую адсорбцию - не более 0 5 мкмолъ / м) или же по обратимости, присущей физической адсорбции. Однако оба эти критерия не являются абсолютными. [41]
Одним из возможных критериев такого различия может служить величина теплоты адсорбции или смачивания. Поэтому при выборе адсорбента бывает полезно предварительное определение теплот адсорбции веществ разделяемой смеси из данного растворителя. Различие в величинах теплот адсорбции изучаемых веществ связано с различием их ад-сорбируемости и может поэтому дать ценные указания при выборе адсорбента. [42]
Но строение решетки может влиять не только на величину теплоты адсорбции, но и на энергию активации. [43]
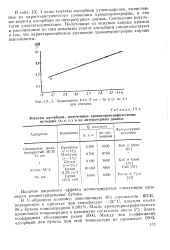 |
Зависимость 10GO / T от - In ц ( г. ж. х. для гептана. [44] |
Полученные из опытных данных прямые и рассчитанные по ним величины теплот адсорбции свидетельствуют о том, что характеристическое уравнение хроматермографии хорошо выполняется. [45]
Страницы: 1 2 3 4