Величина - энтальпии - образование
Cтраница 1
 |
Энтальпии образования комплексных солей. [1] |
Величины энтальпии образования, полученные нами, в пределах от 1 до 2 ккал. Причина этого расхождения может быть связана с недостаточной точностью измерения изменения температуры в калориметре или с методом синтеза и анализа координационных соединений. Использование термистора для измерения температуры позволяет с большей точностью измерять малые величины энтальпии растворения, которые характерны для рассматриваемых соединений. [2]
Величина энтальпии образования гексанитроэтана 28 6 1 9 ккал / моль вычислена в работе Нобла с соавторами [10] по теплоте сгорания гексанитроэтана в смеси с бензойной кислотой. [3]
Обсудите величины энтальпии образования двуокисей, гексафторидов и кислородных кислот серы, селена и теллура с учетом положения этих элементов в периодической системе ( см. обсуждение устойчивости брома в высших степенях окисления, проведенное в конце разд. [4]
Важно подчеркнуть разницу между величинами энтальпии образования и энергии связи. [5]
Подобным же образом может быть рассчитана непосредственно неопределяемая величина энтальпии образования монооксида углерода СО. [6]
Для каждого вещества можно экспериментально определить величину энтальпии образования одного моля и величину энтропии одного моля. Изменение энтальпии ДЯ при реакции равно разности между суммой энтальпий образования конечных продуктов и суммой энтальпий образования исходных веществ. Аналогично вычисляется и AS реакции. [7]
Однако нужно четко представлять, что в ответственных случаях для суждения о величине энтальпии образования необходим эксперимент, ибо расчетные методы, как правило, не могут обеспечить вполне надежных результатов с хорошей точностью. [8]
 |
Вторые вириальные коэффициенты смесей хлороформ-диэти-ловый эфир при различных температурах. [9] |
Приходится сделать целый ряд предположений об изменении статистической суммы при димеризации, однако вычисления приводят к разумной величине энтальпии образования Н - связи. [10]
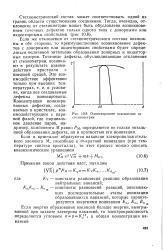 |
Одностороннее отклонение от. [11] |
Если же отклонения от стехиометрического состава возможны в обе стороны, то преимущественное возникновение дефектов с донорными или акцепторными свойствами будет определяться величиной энтальпии образования донорных и акцепторных центров. Точечные дефекты, обусловливающие отклонения от стехиометрии, возникают в результате взаимодействия кристалла с внешней средой. Концентрация ионизированных дефектов, созда - А ваемых в кристалле, взаимодействующем с паровой фазой, где парциаль - стехиометрии ное давление паров, например, компонента М равно РМ, определяется не только энтальпией образования дефекта, но и кратностью его ионизации. [12]
На основании измерения давления пара они установили, что энтальпия испарения при 298 К равна 10 70 ккал / молъ; основываясь на этом значении в сочетании с величиной энтальпии образования жидкого гидразина согласно работе Хьюза, Корручини и Джиль-берта [658], они определили Д / 98 ( g) 22 75 ккал / молъ. [13]
На основании измерения давления пара они установили, что энтальпия испарения при 298 К равна 10 70 ккал / молъ; основываясь на этом значении в сочетании с величиной энтальпии образования жидкого гидразина согласно работе Хьюза, Корручини и Джиль-берта [658], они определили Д / 98 ( g) 22 75 ккал / молъ. [14]
На основании измерения давления пара они установили, что энтальпия испарения при 298 К равна 10 70 ккал / молъ; основываясь на этом значении в сочетании с величиной энтальпии образования жидкого гидразина согласно работе Хьюза, Корручини и Джиль-берта [658], они определили ДЯ / 98 ( g) 22 75 ккал / молъ. [15]
Страницы: 1 2 3