Величина - энтропия
Cтраница 1
Величина энтропии ( S) какого-либо соединения при данной температуре зависит от того, какие колебательные, вращательные и поступательные движения могут совершать атомы, входящие в состав молекулы этого соединения. [1]
Величина энтропии указывает среднее число двоичных знаков ( см. Двоичная единица), необходимое для различения ( записи) возможных значений случайной величины. Это обстоятельство позволяет понять роль количества И. Если случайные величины X и Y независимы, то для записи значения X требуется в среднем Я ( X) двоичных знаков, для записи значения У требуется Я ( У) двоичных знаков, а для пары ( X, У) требуется Я ( Х) Н ( У) двоичных знаков. [2]
Величина энтропии характеризует вероятность состояния и поэтому может быть использована для предсказания направления процессов. [3]
Величина энтропии зависит от абсолютной температуры. [4]
Величина энтропии при состоянии газа в этих условиях считается равной нулю. [5]
Величина энтропии, определенная калориметрическим методом, удовлетворительно согласуется с коррелированными функциями, отобранными Россини, Питцером, Арнеттом, Брауном и Пи-ментелом [1248]; ради соответствия приняты эти коррелированные функции и энтальпия образования. [6]
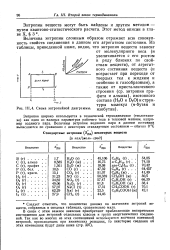 |
Схема энтропийной диаграммы. [7] |
Величина энтропии сложным образом отражает всю совокупность свойств соединения в данном его агрегатном состоянии. [8]
Величина энтропии сложным образом отражает всю совокупность свойств соединения в данном агрегатном состоянии. [9]
 |
Расчет энтропии этилена при 298 К и 1 атм. [10] |
Величина энтропии сложным образом отражает всю совокупность свойств соединения в данном агрегатном состоянии. [11]
Величина энтропии указывает среднее число двоичных знаков, необходимое для различения ( или записи) возможных значений случайной величины. Это обстоятельство позволяет понять роль количества И. Я ( т)) двоичных знаков, а для пары (, т)) требуется Я () Я ( т ]) двоичных знаков. [12]
Величины энтропии и теплоты реакции могут быть измерены, например, калориметрическим способом, и определение изменения свободной энергии или изобарного потенциала, а, следовательно, и константы равновесия возможно произвести, не прибегая к каким-либо химическим измерениям. Такого рода расчеты химического равновесия представляют особый интерес для органической химии, где часто не имеется других методов определения константы равновесия вследствие медленности протекания реакции и невозможности прямых измерений равновесия. [13]
Величина энтропии сложным образом отражает всю совокупность свойств соединения в данном его агрегатном состоянии. Из таблицы, приведенной ниже, видно, что энтропия веществ зависит от молекулярного веса ( и увеличивается с его ростом в ряду близких по свойствам веществ), от агрегатного состояния веществ ( и возрастает при переходе от твердых тел к жидким и особенно к газообразным), а также от кристаллического строения ( ср. [14]
Величина энтропии указывает среднее число двоичных знаков, необходимое для различия ( или записи) возможных значений случайной величины. Это обстоятельство позволяет понять роль количества информации при хранении ее в запоминающих устройствах измерительных систем. Если случайные величины Хи Y независимы, то для записи значения X требуется в среднем Н ( X) двоичных знаков, для значения Y требуется Н ( Y) двоичных знаков, а для пары ( X, Y) требуется Н Х) H Y) двоичных знаков. [15]
Страницы: 1 2 3 4