Бромистый алюминий
Cтраница 1
Бромистый алюминий образуется в виде белого дыма. С кислородом бром непосредственно не реагирует. [1]
Бромистый алюминий ( кислота Льюиса) путем элиминирования из молекулы углеводорода гидрид-иона образует ион карбония. [2]
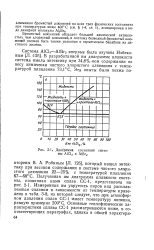 |
Диаграмма состояния системы А1С1а и А ] Вг3. [3] |
Бромистый алюминий обладает большей химической активностью, чем хлористый алюминий, и поэтому безводный бромистый алюминий должен быть также упакован а герметичном барабане из ли-стовлго железа. [4]
Бромистый алюминий ( бромид алюминия) представляет собой бесцветные кристаллы, уд. Бромистый алюминий хорошо растворяется в органических растворителях и в жидком броме. Он дымит на влажном воздухе вследствие образования бромистого водорода. [5]
Бромистый алюминий легко растворяется в ароматических углеводородах с образованием окрашенных растворов. Поэтому представляется вероятным, что имеется тенденция возрастания диссоциации димера с увеличением основных свойств ароматического углеводорода. [6]
Бромистый алюминий ( бромид алюминия) представляет собой бесцветные кристаллы, уд. Бромистый алюминий хорошо растворяется в органических растворителях и в жидком броме. Он дымит на влажном воздухе вследствие образования бромистого водорода. [7]
Бромистый алюминий обработан кислородом ( 170 мл в пересчете на нормальные условия) при 20 - 25 в течение 476 час. [8]
Бромистый алюминий оказался значительно более эффективным катализатором, вызывающим разложение н-пентана, и для того чтобы вызвать реакцию, не требовалось преднамеренно вводить в реакционную смесь посторонние вещества. Установлено, что 14-пентан, содержащий 1 5 % ( мол. Количества образующихся бутанов возрастали с течением реакции практически линейно, а количество изопентана достигало максимума, от которого слабо отклонялось по мере дальнейшего проведения реакции. [9]
Бромистый алюминий ( типичная кислота Льюиса) путем элиминирования из молекулы углеводорода гидрид-иона способствует образованию иона карбония. Образование иона карбония сопровождается перегруппировкой, включающей миграцию заместителя R; затем путемприсоединения гидрид-иона возникает углеводород, изомерный исходному. Эти достаточно хорошо известные представления необходимо дополнить некоторыми соображениями, весьма важными для механизма реакций циклических насыщенных углеводородов. [10]
Жидкий бромистый алюминий и его пары, Таким образом, входят в контакт с избытком алюминия, который служит для удаления избытка брома. [11]
Бромистому алюминию было отдано предпочтение перед хлористым алюминием потому, что его растворимость в углеводородах допускает начало гомогенной реакции. Реакция была проведена в сосуде, который был предварительно эвакуирован, прогрет и продут не содержавшим кислорода азотом. [12]
Если бромистый алюминий заместить хлористым, то число, род и устойчивость комплексов будут те, которые свойственны его хлористому соединению. Однако при применении солей металла, который стоит ниже в электрическом ряду, как, например, хлористая сурьма, образующиеся комплексы являются в меньшем числе и в менее устойчивом состоянии. [13]
Вместо бромистого алюминия может быть использовано бромное железо. [14]
 |
Зависимость сдвигов частот. [15] |
Страницы: 1 2 3 4