Размер - анион
Cтраница 2
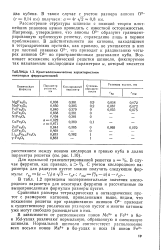 |
Кристаллохимические характеристики некоторых феррошпинелей. [16] |
В таком случае с учетом размера аниона О2 - ( 0 14 нм) получаем: а 4г л / 2 0 8 нм. [17]
Чем больше отрицательный заряд и меньше размер аниона, тем легче протон отрывается от молекулы воды. Оторвавшийся протон присоединяется к аниону. [18]
Однако изменение температуры также влияет на размеры комплексообразую-щего аниона ( вследствие изменения колебательного движения его атомов) и в связи с этим на избирательность комплексообразования. [19]
Какая зависимость существует между зарядом и размером аниона и его склонностью к гидролизу. [20]
 |
Константы скорости реакции гидролиза бромалканов RBr OH - - ROH Br - ( 80 % - ный этанол, 55 СС. [21] |
Нуклеофильность увеличивается при увеличении поляризуемости реагента, размера аниона. Реакции способствуют полярные растворители, которые не образуют водородные связи ( гл. [22]
Понятно, что чем более отрицательный заряд и меньше размер аниона, тем он более сильный донор электронных пар и тем легче отрывает протон от молекулы воды. [23]
Понятно, что чем больше отрицательный заряд и меньше размер аниона, тем он более сильный донор электронных пар и тем легче отрывает протон от молекулы воды. [24]
Очевидно, что чем больше отрицательный заряд и меньше размер аниона, тем он более сильный донор электронных пар и тем он легче отрывает протон от молекулы воды. [25]
Понятно, что чем больше отрицательный заряд и меньше размер аниона, тем он более сильный донор электронных пар и тем легче отрывает протон от молекулы воды. [26]
Понятно, что, чем больше отрицательный заряд и меньше размер аниона, тем легче осуществляется этот процесс. [27]
Основными влияющими на эту экстракцию факторами является сила кислоты, размер аниона и его гидрофильная или гидрофобная природа. [28]
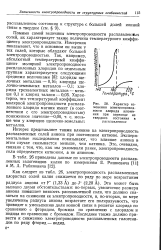 |
Характер изменения электропроводности хлорида алюминия при переходе из твердого состояния в расплавленное. [29] |
Это может быть вызвано двумя обстоятельствами: во-первых, увеличение размера аниона повышает вязкость расплавленной соли, что должно сказаться на снижении ее электропроводности, и, во-вторых, по мере увеличения радиуса аниона возрастает его поляризуемость, что приводит к уменьшению доли ионной связи в решетке хлорида по сравнению с фторидом, бромида по сравнению с хлоридом и иодида по сравнению с бромидом. Последнее также должно привести к снижению электропроводности расплавленных галогенидов по ряду фторид - иодид. [30]
Страницы: 1 2 3 4 5