Размер - анион
Cтраница 4
Вычисленные значения ср несколько более постоянны, чем в случае гексафторосиликатов, так как из-за меньшего заряда и размера аниона уменьшается поляризационное взаимодействие. Однако и в этом случае точность вычисленных теплот диссоциации тетрафтороборатов двухвалентных металлов остается низкой. Если, как указано выше, энтальпия диссоциации KBF4, а также и других тетрафтороборатов щелочных металлов, на 11 - 13 ккал выше величины, использованной в таблице, то соответственно увеличивается и о, а вычисленная теплота образования двухвалентных тетрафтороборатов должна быть увеличена на 22 - 26 ккал. Этот вопрос нуждается в дальнейших исследованиях. [46]
Соли тетраалкиламмония, напротив, ускоряют обмен, причем наибольший эффект наблюдается в случае хлорида тетраалкиламмония; с увеличением размера аниона галоида подобное действие уменьшается. Скорость литий-галоидного обмена определяется как специфической, так и неспецифической сольватацией растворителем и подчиняется закономерностям диполь-дипольного взаимодействия, что, как считают авторы этого исследования [197], исключает как ионный, так и радикальный механизмы. [47]
Однако для большинства составов бинарной системы расплавленных окислов таких резких изменений ожидать нельзя из-за отсутствия в смеси небольших по размеру анионов. Следовательно, давление пара всегда сравнительно велико, и знание его в зависимости от содержания компонентов не позволяет сделать однозначные выводы о структуре жидкости. [48]
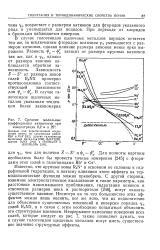 |
Средние моляльные. [49] |
В случае галогенидов щелочных металлов порядок остается тем же, за исключением фторидов: величина у уменьшается с размером катионов, однако влияние размера анионов менее ярко выражено. Разность фа - j v зависит от размера крупных катионов так же, как и у, однако от размера анионов наблюдается обратная зависимость. [50]
В бинарных соединениях, образованных компонентами с общим катионом, но разными анионами, по-видимому, действует правило: чем больше разница в размерах анионов, тем больший вклад в состав образующихся соединений вносит меньший по размерам анион. [51]
Приведенный выше анализ уравнения изотермы сокри-сталли зации ( уравнение 4) позволяет сформулировать следующее правило: сокристаллизация соединений уменьшается с увеличением молекулярной массы макрокомпонента, размеров общего аниона, энтропии растворителя, а также с ослаблением химических связей в молекулах соединений. [52]
Если не принимать во внимание специфических свойств ионов, обусловленных конфигурацией их электронных оболочек, то решающим для координации фактором является отношение размера катиона к размеру аниона. Силы электростатического притяжения действуют лишь на очень малых расстояниях между катионом и окружающим этот катион анионами, вследствие чего ионный радиус катиона должен иметь по крайней мере такую же величину, как и радиус сферы, вписанной в пространство внутри координационного многогранника. Однако если катион слишком велик, то выгоднее становится более высокое координационное число, которое соответствует более плотному расположению анионов, а следовательно, и более полной нейтрализации заряда катиона. Если представить себе анионы просто как недеформируемые шары, то можно ожидать, что верхняя граница для величины катионного радиуса при заданном координационном числе приблизительно определяется минимальным радиусом катиона, соответствующим следующему более высокому значению координационного числа. [53]
Влияние строения кетона может проявиться на первой стадии процесса в связи с реакционной способностью находящегося в а-положении водородного атома, на второй стадии - в связи с основностью и размерами аниона кетона и на третьей - в связи с кислотностью образующегося Р - дикетона. В общем случае легкость ацилирования кетонов сложным эфиром и основанием падает при переходе к кетонам менее простого строения. [54]
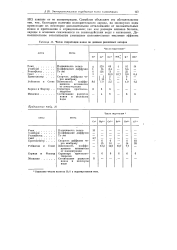 |
Числа гидратации ионов по данным различных авторов. [55] |
Самойлов объясняет это обстоятельство тем, что, благодаря наличию положительного заряда, на молекулах воды происходит их некоторое дополнительное отталкивание от положительных ионов и притяжение к отрицательным; так как размеры анионов больше, заряды в основном сказываются на взаимодействии воды с катионами. [56]
 |
Ионные радиусы неметаллических элементов. [57] |
Другими словами, большой ионный заряд иона С вызывает значительное изменение сил, с которыми положительно заряженное ядро противодействует отталкиванию между электронами, и именно этим объясняется столь большое различие в размерах анионов углерода и иода. [58]
Большая нуклеофильность М - по сравнению с M Y -, вытекающая из приведенных выше данных, является отражением меньшей степени поляризации Y - в SSIP и того факта, что в переходном состоянии 31 она снижается в меньшей степени с увеличением размера аниона. [59]
Принцип плотнейшей кладки остается справедливым и для ионных химических соединений. Размеры анионов, как правило, значительно больше размеров катионов. В ионных структурах анионы располагаются по одному из законов плотнейшей кладки, катионы же располагаются в промежутках между анионами, в пустотах. Но катионы обычно не заполняют всех пустот между анионами. [60]
Страницы: 1 2 3 4 5