Размер - анион
Cтраница 3
Эти эксперименты показывают, что скорость окклюзии соли зависит от размера гостевого аниона и что для галогенид-ионов величина, соответствующая насыщению окклюзии, составляет один галогенид-ион на содалитовую ячейку. На скорость окклюзии существенно влияет размер аниона: хлорид-ионы ( диаметр 3 4 А) легко заполняют ячейки при 550 С, в то время как иодид-ионы ( диаметр 5 4 А) даже при 700 С заполняют ячейки только частично. [31]
Поскольку устойчивость мостика М ОН Х - Н увеличивается с уменьшением размера аниона, его существование противоречит принципу Шварца [505], согласно которому уменьшение размера противо-иона снижает устойчивость SSIP по отношению к CIP за счет увеличения силы, выталкивающей растворитель. [32]
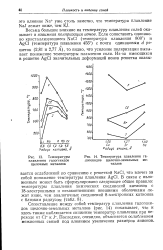 |
Температура плавления галогенидов щелочно-земельных металлов. [33] |
Последнее, очевидно, объясняется ослаблением межионных связей под влиянием увеличения размеров анионов. [34]
Повышению указанной выше экзотермичности процесса смешения в жидкой фазе благоприятствует увеличение размеров общего аниона сокристаллизующихся компонентов, увеличение различия между конфигурацией ионов макрокомпонента и ячейками тетраэд-рической структуры воды. [35]
В металлах все сферы имеют, одинаковый размер, но в солях размеры аниона часто значительно превосходят размеры катиона. Поэтому для таких ионных решеток характерна ллотная упаковка анионов, в пустотах между которыми размещаются катионы. В хлористом натрии, например, каждый ион хлора окружен шестью ионами натрия и наоборот ( рис. 8), следовательно, здесь координация равна шести, так же как и для решеток КВг и KJ. В решетках СаВг2 и CsCl с координационным числом 8 ионы металлов окружены восемью ионами брома или хлора каждый. [36]
 |
Температуры плавления. [37] |
Из этих данных отчетливо видна общая тенденция снижения температуры плавления с увеличением размеров анионов. Наибольший интерес вызывает тот факт, что NalAl ( октил) 41 является при комнатной температуре жидкостью, хотя данные, полученные при изучении электропроводности, свидетельствуют о том, что это соединение является ионным. [38]
В этом случае наблюдается лишь незначительное изменение ионных радиусов, поскольку увеличение размеров анионов вследствие уменьшения порядкового номера в значительной степени компенсируется сжатием этих анионов под воздействием возросших кулоновских сил. [39]
Давно установлено, что устойчивость низшего галогенида к диспропорционированию обычно растет с возрастанием размера аниона. Ртуть ( 1) и кадмий ( I) являются исключениями. [40]
Общая молярная либрационная интенсивность в области 440 - 780 см-1 возрастает с увеличением размера аниона ( Вг - С1 -) и линейно возрастает с увеличением концентрации галогенидов щелочного металла. [41]
Для всех солей типа R4NX величина, как правило, уменьшается с возрастанием размера анионов. [42]
Соединения типа MX-это своеобразные двумерные металлы, связь М - М в которых зависит от размера аниона, например г ( ТЬ-ТЬ) в TbCl равно 3 79, в ТЬВг-384 А. Отсутствие монойодидов РЗМ поэтому может быть приписано чрезмерному удлинению связи Ln-Ln в этом случае. [43]
 |
Кристаллическая структура анионного криптата [ ciLH ] 3 ( L-сферический трициклический криптанд 43 (, воспроизведено с любезного разрешения American Chemical Society. [44] |
Эти результаты показывают, что структура, представленная на рис. 3.42, устойчива благодаря топологическому соответствию размера аниона величине прлости криптанда. [45]
Страницы: 1 2 3 4 5