Размещение - молекула
Cтраница 3
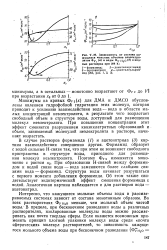 |
Зависимость от состава кажущихся мольных объемов неэлектролитов Фу2 ( а и воды Фу pj2o ( в водных растворах при 298 К. [31] |
Минимумы на кривых vz ( x) Для ДМА и ДМСО обусловлены явлением гидрофобной гидратации этих молекул, которая приводит к усилению взаимодействия вода - вода в области малых концентраций неэлектролита, в результате чего возрастает свободный объем в структуре воды, доступный для размещения молекул неэлектролита. При повышении концентрации этот эффект сменяется разрушением квазиклатратных образований и объем, занимаемый молекулой неэлектролита в растворе, начинает возрастать. [32]
При охлаждении расплавленных веществ могут образоваться кристаллы или стекла. Размещение молекул ( атомов, ионов) в кристаллической решетке возможно только тогда, когда частицы еще обладают определенной подвижностью, зависящей от их размеров и соотношения между тепловым движением и энергией межмолекулярного взаимодействия. По мере падения температуры быстро возрастает вязкость, что еще больше затрудняет перемещение и взаимную ориентацию частиц; наконец, наступает момент, когда тепловое движение уже ке может обеспечить протекание этих процессов. Следовательно превращение жидкости в стеклоподобное тело не сопровождается фазовым переходом. [33]
 |
Схематическое изображение структуры воды при внесении в нее углеводорода ( по Немети и Шераге. [34] |
Так как при этом выпуклая поверхность почти сферического кластера становится вогнутой, то поверхностные молекулы воды могут образовывать максимальное число водородных связей с соседями - четыре. Размещение молекул углеводорода в районах несвязанной воды может происходить только заменой контактов вода - вода контактами вода - углеводород. [35]
Интересно, что такое расположение очень далеко от наиболее плотной укладки молекул. Это происходит потому, что при размещении молекул в более плотной структуре не могла бы сохраниться такая их взаимная ориентация, которая отвечает тетраэд-рическому распределению четырех связей кислородного атома и которая необходима для возникновения водородной связи. Искажение же валентных углов требует затраты значительного количества энергии. Всем этим объясняется рыхлая структура льда и тот факт, что плотность льда меньше, чем плотность жидкой воды. [36]
Интересно, что такое расположение очень далеко от наиболее плотной укладки молекул. Это происходит потому, что при размещении молекул в более плотной структуре не могла бы сохраниться такая их взаимная ориентация, которая отвечает тетра-эдрическому распределению четырех связей кислородного атома и которая необходима для возникновения водородной связи. Искажение же валентных углов требует затраты значительного количества энергии. Всем этим объясняется рыхлая структура льда и тот факт, что плотность льда меньше, чем плотность жидкой воды. В состав ионных кристаллов могут входить и некоторые нейтральные молекулы, достаточно малые по размеру и обладающие значительной полярностью или способностью к образованию донорно-акцепторной связи или водородной связи. Это относится главным образом к молекулам воды и в меньшей степени к молекулам аммиака. [37]
Представление об энтропии, как мере неупорядоченности, позволяет нам уяснить зависимость энтропии не только от температуры, но и от объема. При сокращении объема газа упорядоченность в размещении молекул растет, число возможных микросостояний становится меньше, уменьшается при этом и энтропия. [38]
 |
Структура льда. [39] |
Интересно, что такое расположение очень далеко от наиболее плотной укладки молекул. Это происходит потому, что при размещении молекул в более плотной структуре не могла бы сохраниться такая их взаимная ориентация, которая отвечает тетра-эдрическому распределению четырех связей кислородного атома и которая необходима для возникновения водородной связи. Искажение же валентных углов требует затраты значительного количества энергии. Всем этим объясняется рыхлая структура льда и тот факт, что плотность ль а меньше, чем плотность жидкой воды. [40]
 |
Структура льда ( заштрихованные круги представляют водородные атомы данной молекулы. черные - связи ее кислорода с водородными атомами соседних молекул. [41] |
Интересно, что такое расположение очень далеко от наиболее плотной укладки молекул. Это происходит потому, что при размещении молекул в более плотной структуре не могла бы сохраниться такая их взаимная ориентация, которая отвечает тетраэдрическому распределению четырех связей кислородного атома и которая необходима для возникновения водородной связи. Искажение же валентных углов требует затраты значительного количества энергии. Всем этим объясняется рыхлая структура льда и тот факт, что плотность льда меньше, чем плотность жидкой воды. [42]
Для кристаллизующихся низкомолекулярных соединений под дальним порядком понимается закономерное расположение основных звеньев на расстояниях больших, чем размеры молекулы. При ближнем порядке наблюдается упорядоченность в размещении близко расположенных молекул. [43]
Минимальная энергия, необходимая для того, чтобы молекула жидкости ( или твердого тела) могла переместиться из одного временного положения равновесия в другое, называется энергией активации самодиффузии. Величина этой энергии q зависит от степени упорядоченности размещения молекул и от величины межмолекулярных сил. [44]
Однако эти представления, согласующиеся с общими представлениями о природе высокоэтастичности и других свойств полимеров, подвергнуты, последние годы серьезному пересмотру, так как более глубокий физический анализ показывает, что полностью хаотического расположения макромолекул з полимерных телах быть не может. Даже з пизкомолекулярных жидкостях с асимметричными молекулами отчетливо наблюдается упорядоченность з размещении близко расположенных молекул. Для длинных лепных молекул это стремление к упорядоченности в аморфном состоянии должно быть выражено гораздо резче. Кроме того, невозможно представить даже чисто геометрически ( при учете определенных межатомных расстоянии и валентных углов) такую картину хаотически перепутанных цепных молекул, которая согласовывалась бы с наблюдаемыми значениями плотностей полимеров, а также с размерами кристаллических и аморфных областей. [45]
Страницы: 1 2 3 4