Разность - химический потенциал
Cтраница 2
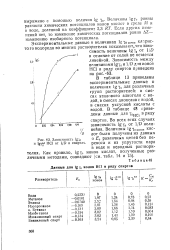 |
Данные для Igf, ионов НС1 в ряду спиртов.| Зависимость lg - ( 0 и Igf9 HC1 от 1 / D в спиртах. [16] |
Величины Igy0 равны разности химических потенциалов ионов кислот в среде М и в воде, деленной на коэффициент 2 3 RT. Если других изменений нет, то изменение химических потенциалов равно AZ - изменению изобарного потенциала. [17]
В случае обратимых электродов разность химических потенциалов, участвующих в электродной реакции ионов на электроде и в растворе, не зависит от наличия специфической адсорбции ионов, в связи с чем потенциал электрода такой же, как в отсутствие специфической адсорбции. [19]
 |
Изменение потенциала в двойном электрическом слое при специфической адсорбции катионов ( а и анионов ( 5. [20] |
В случае обратимых электродов разность химических потенциалов участвующих в электродной реакции ионов на электроде и в растворе не зависит от наличия специфической адсорбции ионов, в связи с чем равновесный потенциал электрода такой же, как в отсутствие специфической адсорбции. [21]
В случае обратимых электродов разность химических потенциалов участвующих в электродной реакции ионов на электроде и в растворе не зависит от наличия специфической адсорбции ионов, в связи с чем равновесный потенциал электрода такой же, как при отсутствии специфической адсорбции. [23]
Движущей силой адсорбции является разность химических потенциалов компонентов в объеме и на поверхности, которые со временем выравниваются. В результате наступает адсорбционное равновесие. [24]
Движущей силой адсорбции является разность химических потенциалов компонентов в объеме и на поверхности, которые в ходе адсорбции выравниваются. В результате наступает адсорбционное равновесие. [25]
Скорость фазовых переходов пропорциональна разности химических потенциалов Гиббса компонента i в фазе / и /, которые зависят от компонентного состава, давления и температуры. [26]
Причиной фазовых превращений является разность химических потенциалов различных фаз. [27]
Процесс протекает под влиянием разности химических потенциалов или парциальных давлений, пропорциональных концентрации диффундирующего вещества ( называемого далее пенетрантом) с обеих сторон мембраны. Проницаемость полимерных пленок обусловлена главным образом активированной диффузией, однако для гетерогенных пленок возможен смешанный механизм из-за фазового проникновения пенетранта в микрополости вокруг частиц наполнителя или крупных кристаллических образований. [28]
Действительно, для углеводородов разности унитарных химических потенциалов (4.40) отрицательны и составляют примерно 3570 Дж / моль СН2 - групп и 8400 Дж / моль CHj-групп. Гидрофобный эффект определяется свойствами воды - гидрофобные вещества безразличны к неполярным органическим растворителям. [29]
Движущая сила, обусловленная разностью химических потенциалов, переносит растворитель через мембрану в трубку. Проникновение растворителя можно объяснить как диффузию под действием градиента концентрации: в результате проникновения растворителя в раствор содержание растворителя х увеличивается и постепенно приближается к 1, хотя не может быть ей равным, сколько бы растворителя ни прошло в трубку, так как в растворе остается исходное количество растворенного вещества. [30]
Страницы: 1 2 3 4

