Разность - энтропия
Cтраница 1
Разность энтропии CH3OD и СН3ОН в жидкой фазе складывается из соответствующих разностей для колебаний, перечисленных в табл. 65, и либрации молекул. [1]
Разность энтропии D20 и Н20 в парообразном состоянии при 298 К, по результатам расчета [424], составляет: ( Д п ( 5в) п - ( 5н) п 2 27 кал / моль - град. [2]
Разность энтропии s2 - 5j может быть определена через теплоту перехода. [3]
Разность энтропии для фторидов переходных металлов отчетливо больше, чем для других, в среднем она близка к семи. [4]
Разность энтропии в двух состояниях вычисляется особенно просто, если обратимый переход из одного состояния в другое происходит при постоянной температуре. Это имеет место, например, при переходах из одного агрегатного состояния в другое. [5]
Разность энтропии CH3OD и СН3ОН в жидкой фазе складывается из соответствующих разностей для колебаний, перечисленных в табл. 6, и либрации молекул. [6]
Разность энтропии D2O и Н2О в паровой фазе при 298 К по результатам расчета [439] составляет ( Д5) п ( S. [7]
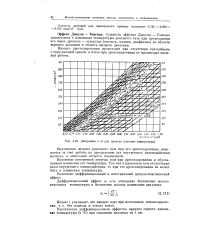 |
Диаграмма t - S для пропана ( высокие температуры. [8] |
Разность энтропии для приведенного примера составляет 0 765 - 0 660 0 105 ккал / кГ град. [9]
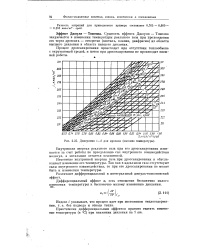 |
Диаграмма i - S для пропана ( высокие температуры. [10] |
Разность энтропии для приведенного примера составляет 0 765 - 0 660 ОД05 ккал / кГ град. [11]
Разность энтропии в начальном и конечном достояниях не зависит от того пути, по которому система пришла из начального состояния в конечное. [12]
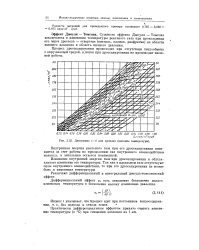 |
Диаграмма z - S для пропана ( высокие температуры. [13] |
Разность энтропии для приведенного примера составляет 0 765 - 0 660 0 105 ккал / кГ град. [14]
Разность энтропии в точках 7 и 5 представляет собой приращение энтропии системы из-за необратимости процесса теплообмена. [15]
Страницы: 1 2 3 4