Разность - энтропия
Cтраница 3
Выражение для разности энтропии двух состояний приобретает особенно простой вид при обратимом изотермическом процессе. [31]
Итак, разности энтропии идеального газа можно легко рассчитать, если известны параметры р и V системы. [32]
Абсолютная величина разности энтропии также максимальна при температуре фазового перехода. Используя эту величину, можно ориентировочно оценить количество выделяемой энергии при фазовом переходе. Оно будет равно около 920 кал / моль, что довольно хорошо согласуется с экспериментальными результатами, полученными непосредственно при изучении теплот сгорания угле-графитовых тел. [33]
По теории Тисса разность энтропии AiS1 должна соответствовать той части теплосодержания жидкости, которая обязана своим происхождением возникновению аномальных возбуждений выше 0 7 К. Теория Ландау, напротив, утверждает, что разность энтропии Д / 51 должна быть в точности равна полной измеряемой энтропии жидкости. [34]
По теории Тисса разность энтропии АЛ1 должна соответствовать той части теплосодержания жидкости, которая обязана своим происхождением возникновению аномальных возбуждений выше 0 7 К. Теория Ландау, напротив, утверждает, что разность энтропии AiS должна быть в точности равна полной измеряемой энтропии жидкости. [35]
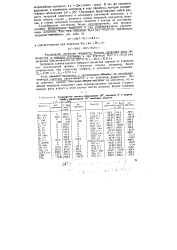 |
Стандартные теплоты образования АН, энтропии S Гиббса образования ЛО некоторых веществ. [36] |
Последние представляют собой разность энтропии конечного и исходного состояний вещества, а в более общем случае - разность суммы энтропии продуктов, реакции и суммы энтропии исходных веществ с учетом их состояния. [37]
Величина Ik равна разности энтропии в пределах одного скачка Ям - Ят, где / / м - верхняя граница ступеньки, Ят - нижняя. Под действием помех Н ( х) меняется в соответствии с изменением дисперсии объекта. [38]
Показать, что разность энтропии системы в состояниях 2 и / ( при условии, что S2Si) может быть определена как наименьшее количество тепла, которое требуется сообщить системе, чтобы квазистатически перевести. [39]
Согласно второму началу разность энтропии St - 50 не зависит от пути и является определенной величиной. [40]
Для переходных металлов разность энтропии фторида и металла может возрасти до 25 - 30 единиц, что уменьшает lg / S1F ( на 2 - 3 единицы, но при этом заметно уменьшается абсолютная величина ДЯ. [41]
Энтропия плавления является разностью энтропии в точках А и С ( рис. 59), изображающих соответственно твердое тело и жидкость, находящиеся при отвечающей данному давлению температуре плавления. [42]
В соответствии с этим разность энтропии при постоянном давлении и постоянном объеме можно рассматривать как константу, слабо изменяющуюся при переходе от металла к металлу. [43]
Экспериментальные методы определения такой разности энтропии рассмотрены в гл. [44]
Железо, потому что разность энтропии в случае окисления тантала не составляет настолько большой отрицательной Величины, чтобы суммарный потенциальный барьер оказался таким же высоким, как барьер, существующий для окисления железа. Эти результаты не соответствуют утверждениям Мак-Адама и Гейла [32], согласно которым тантал окисляется медленнее, чем цирконий и железо. [45]
Страницы: 1 2 3 4