Начальная разность - потенциал
Cтраница 4
По наклону поляризационных кривых на коррозионных диаграммах можно всегда судить о том, какая из электродных реакций определяет суммарную скорость коррозионного процесса, и рассчитать относительную долю начальной разности потенциалов, которая теряется на данном виде сопротивления. Эта величина называется мерой контроля коррозионного процесса данной электродной реакцией или контролирующим фактором. Мерой катодного и анодного контроля могут служить величины тангенсов углов наклона поляризационных кривых аир. [46]
В положении переключателя / 2 ( рис. 150) на клеммах / - / направление магнитного поля в зазоре электромагнита таково, что хол-ловская разность потенциалов U складывается с начальной разностью потенциалов V, обусловленной несколько несимметричным расположением электродов Аг и Л2 на пластинке германия. При изготовлении образцов для измерения эффекта Холла обычно не удается расположить контакты AI и Л2 точно на эквипотенциальной линии. [47]
Степень омического контроля ( см. рис. 106) равна нулю при полной заполяризованности коррозионного элемента, когда сила тока г г тах - Скорость коррозии металла при этом определяется лишь начальной разностью потенциалов и поляризационными характеристиками катодной и анодной стадий. [48]
Из этого уравнения становится ясно, что скорость коррозионного процесса можно увеличить изменением начальных потенциалов катодного и анодного процессов фа и фк или, если речь идет о макроэлементе, увеличением начальной разности потенциалов. Таких же результатов можно добиться, если уменьшить катодную и анодную поляризацию RK и Ra или омическое сопротивление, если оно определяет коррозионный ток. В связи с этим необходимо иметь точное представление о механизме процесса, который воспроизводится в ускоренных испытаниях, и знать, какая электрохимическая реакция его контролирует. [49]
Омическое падение потенциала проявляется в данных условиях лишь в тонких пленках и растет по мере удаления от границы контакта электродов; на расстоянии 0 25 мм оно составляет 1 - 2 % от начальной разности потенциалов, и лишь на расстоянии 10 мм становится соизмеримым с катодным поляризационным сопротивлением. [50]
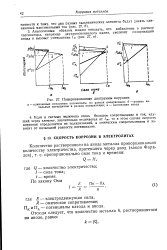 |
Поляризационные диаграммы коррозии. [51] |
Если в систему включено очень большое сопротивление и ток, идущий через элемент, значительно отличается от / м то в этом случае скорость коррозии определяется не поляризацией, а омическим сопротивлением и зависит от начальной разности потенциалов. [52]
В последнем выражении учитывается как поляризационные, так и омическое сопротивления. Согласно ему начальная разность потенциалов коррозионной пары падает на омическом и поляризационном сопротивлениях. [53]
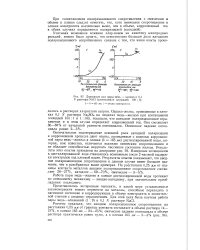 |
Диаграмма для пары медь - железо в 0 1 N растворе NaCl ( соотношение площадей 100. 1. [54] |
Однако опыты, проведенные в пленках 0 1 N раствора Na2S04 на моделях медь-железо при соотношении площадей 100: 1 и 1: 100, показали, что катодное поляризационное ограничение и в этом случае определяет коррозионный ток. Оно составляет 86 - 88 % от начальной разности потенциалов. [55]
Страницы: 1 2 3 4