Разрыв - водородная связь
Cтраница 2
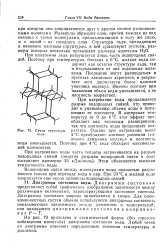 |
Схема структуры льда. [16] |
При нагревании воды продолжается разрыв водородных связей, что приводит к уменьшению объема воды и повышению ее плотности. В интервале температур от 0 до 4 С этот эффект преобладает над тепловым расширением, так что плотность воды продолжает возрастать. [17]
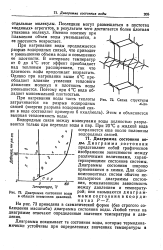 |
Схема структуры льда.| Диаграмма состояния воды в области невысоких давлений. [18] |
При нагревании воды продолжается разрыв водородных связей, что приводит к уменьшению объема воды и повышению ее плотности. В интервале температур от 0 до 4 С этот эффект преобладает над тепловым расширением, так что плотность водь. Однако при нагревании выше 4 С преобладает влияние усиления теплового движения молекул и плотность воды уменьшается. Поэтому при 4 С вода обладает максимальной плотностью. [19]
Хотя при денатурации вследствие разрыва водородных связей и происходит разрушение спиральных структур до беспорядочно свернутых образований, при этом далеко не всегда наблюдается двукратное уменьшение молекулярного веса, которое соответствует разделению двух цепей. Однако необходимо помнить, что определение молекулярного веса часто проводится в условиях, в которых может происходить денатурация ( высокая температура, предельные значения рН, концентрация ДНК и ионная сила ниже 10 - 4 М), и, по-видимому, причина отсутствия изменения в молекулярном весе кроется в том, что при быстром разрушении структуры в какой-то момент была достигнута критическая точка денатурации. В результате этого небольшие участки молекулы, связанные водородными связями, могли переплестись и образовать беспорядочно скрученную структуру, что препятствовало дальнейшему ее разрушению. Из свойств олигонуклеотидов, синтезированных химическим или ферментативным путем, ясно, что участки, состоящие из 3 - 6 пар оснований, связанных водородными связями, имеют достаточные размеры, чтобы препятствовать диссоциации двух цепей. В тех случаях, когда денатурированная ДНК сильно вытянута ( низкая ионная сила), диссоциация возможна. [20]
 |
Зависимость минимально необходимого времени термообработки от обратной температуры. [21] |
Известно, что энергия разрыва водородных связей составляет около 6 0 - 7 1 ккал / моль. То, что полученная величина энергии активации ( 34 7 ккал / моль) примерно в 5 раз больше, показывает, что термическая релаксация волокон из ПВО связана не с разрывом отдельных водородных связей, а с разрушением более сложных структурных образований и с сегментальной подвижностью молекул ПВО в этом процессе. [22]
Энергия, необходимая для разрыва водородных связей при плавлении льда, составляет 6 02 - 0 925 10 кДж - моль-1. Общая энергия водородных связей льда, как рассчитано в примере 9.1, равна 40 кДж - моль-1. [23]
Очень эффективным реагентом для предварительного разрыва водородных связей между макромолекулами целлюлозы и ее активации перед ацилированием является обработка целлюлозных материалов аминами ( см. стр. [24]
Переход, происходящий с разрывом водородных связей, влияет на состояние растворителя, молекулы которого могут стремиться к захвату водородных связей. Таким образом, могут меняться свойства внешней среды, по которой проводится осреднение. [25]
 |
Вязкость ( ц углекислого газа 10 сП [ Голубев И. Ф., Петров В. А., 1953 г. ]. [26] |
При более высоких температурах происходит разрыв водородных связей и образование более плотного расположения молекул. Однако структура надкритического пара, как и воды, изучена недостаточно и пока нет общепринятой структуры, особенно при высоких температурах и давл ениях. [27]
Реакция эндотермична, поскольку для разрыва водородных связей между клубком и ДХУ необходима энергия и поскольку энтропия смешения при освобождении ДХУ превосходит избыток энтропии клубка по отношению к энтропии спирали, так что в результате при образовании спирали энтропия увеличивается. Подобная инверсия возможна только для смеси растворителей. [28]
Какой механизм обеспечивает большие выходы разрыва водородных связей. [29]
Отсюда следует, что энергия разрыва одиночной водородной связи при Т 0 равна 2 87 или 4 38 ккал / моль. Экспериментальное значение А / / для реакции ( RCOOH) 2 ч 2RCOOH в газовой фазе при 400 С составляет 14 65 ккал. Вычитая RТ и разделив на 2, получим экспериментальное значение & Е т при этой температуре, которое равно 6 75 0 15 ккал. Это та энергия, которую нужно затратить для разрыва одиночной связи. [30]
Страницы: 1 2 3 4 5