Различная термодинамическая величина
Cтраница 1
Результаты определения различных термодинамических величин из данных по электродвижущим силам плохо воспроизводимы и очень чувствительны к незначительным изменениям в условиях опыта. Так, если для 1 1-электролита температурный коэффициент электродвижущей силы найден с точностью 0 001 мв / град, то ошибка в определении L2 составляет 7 кал, однако даже из наилучших экспериментальных данных не удается получать столь точных результатов. Если удается довести точность определения L2 до 30 кал, то этот результат можно рассматривать как вполне удовлетворительный. Поскольку относительная точность наилучших калориметрических определений L2 составляет 10 кал, то их следует считать более точными, чем значения, получаемые из данных по электродвижущим силам. [1]
Результаты определения различных термодинамических величин из данных по электродвижущим силам плохо воспроизводимы и очень чувствительны к незначительным изменениям в условиях опыта. Так, если для 1 1-электролита температурный коэффициент электродвижущей силы найден с точностью 0 001 мв / град, то ошибка в определении L2 составляет 7 кал, однако даже из наилучших экспериментальных данных не удается получать столь точных результатов. Если удается довести точность определения L2 до 30 кал, то этот результат можно рассматривать как вполне удовлетворительный. Поскольку относительная точность наилучших калориметрических определений L2 составляет 10 кал, то их следует считать более точными, чем значения, получаемые из данвых по электродвижущим силам. [2]
В критической точке различные термодинамические величины имеют особенности в виде точек ветвления, характер которых представляет значительный физический интерес. После этого возникает идея использовать Паде-метод для того, чтобы найти особую точку и определить характер ветвления. [3]
Поскольку функциональные формы различных термодинамических величин не могут быть с достаточной точностью выведены теоретически, следует рассмотреть интерполяционные формулы. [4]
Через эти суммы и выражают различные термодинамические величины. [5]
Выражение для свободной энергии (19.18) позволяет найти различные термодинамические величины. [6]
Здесь не ставится вопрос о трансформационных свойствах различных термодинамических величин и считается, что мы все время работаем в такой системе отсчета, где в целом газ покоится. Мы ищем лишь новых черт в уравнениях состояния газа, учитывающих, что молекулы или атомы газа движутся с релятивистскими скоростями. [7]
Если свойства системы описываются уравнением, содержащим различных термодинамических величин больше, чем общая вариантность равновесия, то из сказанного выше следует, что некоторые из величин являются функциями других, выбранных в качестве независимых переменных. Уравнения, связывающие одно из внутренних свойств с внешними свойствами и температурой, называют уравнениями состояния. Число независимых уравнений состояния равняется вариантности равновесия, в чем нетрудно убедиться, рассматривая решеАя этих уравнений относительно аргументов. Конкретный вид уравнений состояния термодинамика установить не может, однако вывод об их существовании уже сам по себе позволяет получить некоторые соотношения между свойствами. Так, если закрытая система рассматривается без учета внешних силовых полей и поверхностных. [8]
В физико-химических расчетах [15. 16] широко используется метод нахождения различных термодинамических величин и свойств сложных органических соединений по вкладам вносимых отдельными структурными элементами. [9]
В книге изложены основы термодинамики и связи между различными термодинамическими величинами. Описаны приложения классической и статистической термодинамики к изучению двух - и трехкомпонент-ных металлических растворов. Дан анализ диаграмм состояния сплавов, изложены экспериментальные методы определения теплот растворения, образованчя химических соединений и реакций в жидких и твердых металлических сплавах, методы измерения активностей компонентов и свободных энергий твердых и жидких сплавов. [10]
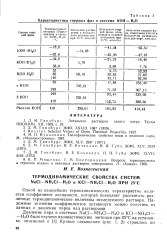 |
Характеристика твердых фаз в системе КОН - Н2О. [11] |
Одной из важнейших термодинамических характеристик является коэффициент активности, который позволяет рассчитать различные термодинамические величины исследуемого раствора. [12]
Формула ( 5 118) имеет общее значение и позволяет вычислять флюктуации различных термодинамических величин. [13]
Наиболее интересной особенностью рассмотренных изотерм является наличие резких изломов, говорящих о скачкообразном изменении различных термодинамических величин. Наличие же критической точки связано с расходимостью различных термодинамических величин, что будет обсуждаться ниже. Главная задача статистической механики состоит в объяснении такого необычного поведения на основе представлений о молекулах, взаимодействующих посредством реалистических сил. [14]
Поэтому для систем, где уравнения ( 233) и ( 234) выполняются, вычисление различных термодинамических величин трудностей не представляет. Однако такие системы на практике встречаются очень редко. [15]
Страницы: 1 2 3