Различная термодинамическая величина
Cтраница 2
Поэтому для систем, где уравнения ( 30) и ( 31) выполняются, вычисление различных термодинамических величин трудностей не представляет. Однако такие системы на практике встречаются очень редко. [16]
В ряде случаев учет переменности давления по высоте столба существен и для других состояний, характеризующихся экстремальными значениями производных различных термодинамических величин ( таких, например, как степень диссоциации и степень ионизации газа) по давлению при Т сопз. [17]
В табл. IX ( заимствованной из работы [39]) для бутанов, пен-танов, гексанов, гептанов приведены значения различных термодинамических величин при 298, 400, 500, 600, 800 и 1000 К. [18]
Вскоре после начала применения электронно-захватного детектора Вентворт с сотрудниками [10-12] в Хьюстонском университете начал изучение пригодности этого детектора для измерения различных термодинамических величин, таких, например, как абсолютное сродство к электрону, и благодаря их работе была значительно развита теория механизма захвата электронов. [19]
Мы приводим здесь вычисления с большей точностью, чем это обычно требуется, имея в виду выявить более ясно взаимоотношение между различными термодинамическими величинами. [20]
Метод этот заключается в том, что на основании соответствующих уравнений состояния и опытных данных, полученных при исследовании разных веществ, строятся графики зависимости различных термодинамических величин от приведенных давления и температуры. [21]
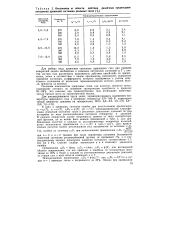 |
Отклонения от области действия различных предпосылок построения уравнений состояния реальных газов ( %. [22] |
Для выбора вида уравнения состояния природного газа при решении конкретной задачи необходимо в заданных интервалах состояний р, Т с учетом состава газа рассмотреть возможность действия какой-либо из предпосылок, затем в соответствии с видом предпосылки рассмотреть конкретное уравнение состояния, коэффициенты которого подбираются с учетом допустимого отклонения от различных термодинамических величин данной модели, принятых за базовые. [23]
Теперь кратко рассмотрим конечноразмерный скейлинг вблизи фазового перехода второго рода. Отметим, что различные термодинамические величины малой системы, слабо взаимодействующей со средой, хорошо определены только в среднем. Их мгновенные значения флуктуируют. [24]
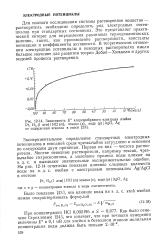 |
Зависимость Е хлорсеребряного электрода ячейки Pt, Н2 ( 1 атм НС1 ( т, этанол ( х, вода ( у AgCl, Ag от содержания этанола в смеси. [25] |
Для полного исследования системы растворенное вещество - растворитель необходимо определить ряд электродных потенциалов при стандартных состояниях. Это представляет практический интерес для определения различных термодинамических величин, таких, как произведение растворимости, константы ионизации и коэффициенты активности. [26]
Теория масштабной инвариантности [1-4] как метод изучения критических явлений получает в последнее время все большее распространение. Она дает связь между критическими индексами различных термодинамических величин, выявляя тем самым главную особенность этих величин при приближении к критической точке. [27]
Для полного исследования системы растворенное вещество - растворитель необходимо определить ряд электродных потенциалов при стандартных состояниях. Это представляет практический интерес для определения различных термодинамических величин, таких, как произведение растворимости, константы ионизации и коэффициенты активности. [28]
Наиболее интересной особенностью рассмотренных изотерм является наличие резких изломов, говорящих о скачкообразном изменении различных термодинамических величин. Наличие же критической точки связано с расходимостью различных термодинамических величин, что будет обсуждаться ниже. Главная задача статистической механики состоит в объяснении такого необычного поведения на основе представлений о молекулах, взаимодействующих посредством реалистических сил. [29]
Для полного исследования системы растворенное вещество - растворитель необходимо определить ряд электродных потенциалов для стандартных состояний. С практической стороны это представляет интерес для определения различных термодинамических величин, таких, как произведение растворимости, константы ионизации и коэффициенты активности. [30]
Страницы: 1 2 3