Распад - озон
Cтраница 3
Сущность процесса обеззараживания воды озоном заключается в окислении бактерий атомарным кислородом, образующимся при распаде озона. Озон одновременно уменьшает цветность, запахи и привкусы воды. [31]
 |
Концентрация озона в зависимости от высоты полета. [32] |
Для защиты органических материалов хорошие результаты дают антиозонан-ты и покрытия, содержащие металлы - катализаторы распада озона и др. Современная химия дает возможность практически полностью устранить воздействие озона на конструкции и детали самолета. [33]
По обеим этим причинам теория, пользующаяся подобием полей, применима к горению окиси углерода или распаду озона и неприменима к горению водорода. [34]
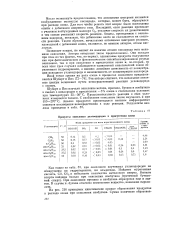 |
Продукты окисления углеводородов в присутствии озона. [35] |
Могло возникнуть предположение, что активными центрами являются возбужденные молекулы кислорода, которые, может быть, образуются при распаде озона. Для того чтобы решить этот вопрос были поставлены опыты с добавками инертного газа. Последний, если реакция протекает с участием возбужденных молекул 02, увеличит скорость их дезактивации и тем самым уменьшит скорость реакции. Опыты, проведенные с окислением водорода, показали, что добавление азота не сказывается на скорости реакции. Таким образом, начальными активными центрами реакции, проводимой с добавками озона, являются, по мнению авторов, атомы кислорода. [36]
В качестве средства борьбы с биологическими обрастаниями все шире применяют озонирование воды, имеющее ряд преимуществ перед хлорированием: продолжительность распада озона ограничена минутами, действие озона на биологические компоненты обрастания в 15 - 20 раз сильнее действия хлора. [37]
Следовательно, в формуле (2.66) и уравнении (2.67) и следующих за ним под No, следует понимать концентрацию кислорода, получившегося при распаде озона, а не полную концентрацию кислорода. [38]
Следовательно, в формуле (2.66) и уравнении (2.67) и следующих за ним под No, следует понижать концентрацию кислорода, получившегося при распаде озона, а не полную концентрацию кислорода. [39]
Один из этих циклов тесно примыкает к проблеме точных значений констант - это новые измерения констант скорости реакции СО с атомами кислорода, элементарных актов распада озона и других реакций. [40]
При добавлении раствора UO в 18 3 М H SO4 в присутствии озона происходит вспышка света, переходящая в медленно спадающее постоянное свечение, обусловленное ХЛ-реакцией распада озона. Более интенсивная вспышка света наблюдается при последующем добавлении в раствор мелкодисперсной элементарной серы, вследствие протекания ХЛ-реакции окисления серы озоном. Вспышка свечения практически отсутствует при добавлении порошка серы к раствору, не содержащему озона. [41]
Филлипс и Шифф [ 45, Ь ] при исследовании взаимодействия активного азота с озоном наблюдали, что добавление N0 ( эффективного дезактиватора колебательно-возбужденных N2) приводит к замедлению распада озона. [42]
Филлипс и Шифф [ 45, Ь ] при исследовании взаимодействия активного азота с озоном наблюдали, что добавление N20 ( эффективного дезактиватора колебательно-возбужденных N2) приводит к замедлению распада озона. [43]
Показано, что в зависимости от кислотности среды в нем преобладают два пути: гетеролитический ( в кислых средах) и гемолитический ( в щелочных средах), инициированный гомогенно-каталитическим распадом озона в присутствии гидроксильных радикалов. [44]
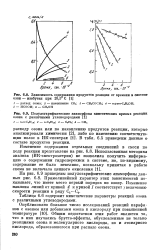 |
Зависимость содержания продуктов реакции от времени в системе озон - изобутан при 28 5 С.| Полулогарифмические анаморфозы кинетических кривых реакции озона с различными углеводородами. [45] |
Страницы: 1 2 3 4