Расположение - атом - кислород
Cтраница 1
Расположение атомов кислорода во всех этих трех фазах не представляет собой правильную упаковку, а напоминает ряд произвольно размещенных групп упругих сфер, подобных тем, которые допускает динамическая теория плотной жидкости или твердого тела, обладающих временными структурами, образованными при удалении из них части сфер. Нет необходимости говорить, что такое расположение атомов не является случайным, а представляет собой структуру твердого кристалла, упорядоченную при определенных температурах и несколько напоминающую либо структуру D0g, либо структуру скалывания, полученную из нее, но в обоих случаях анионы имеют правильную упаковку. [1]
Расположение атомов кислорода в структуре гексагонального льда I представлено на рис. 16 ( Вэлли, 1969), где особенно хорошо видна ажурная структура кристалла льда с большими коридорами. Величина каналов, параллельных оси С, допускает движение по ним атома с радиусом 1 2 А. [2]
Такое расположение атомов кислорода обусловливает наличие в структуре широких каналов. Пустоты в этих каналах таковы, что в них могут размещаться шары, диаметр которых равен диаметру шаров, из которых построены стенки канала. Начало плавления льда есть процесс, при котором молекулы воды проваливаются в каналы. Этим обстоятельством объясняется всем известная аномалия удельного веса льда и воды. [3]
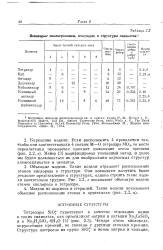 |
Некоторые многогранники, входящие в структуры силикатов а. [4] |
Такие модели отражают расположение атомов кислорода в структуре. Они позволяют получить более реальное представление о структурах, однако строить такие модели значительно труднее. [5]
Пожалуй, более важно учитывать расположение атомов кислорода в соединении, чем их число. [6]
В 1929 г. Бэрнс исследовал расположение атомов кислорода в кристалле льда I с помощью дифракции рентгеновских лучей и показал, что атомы кислорода в кристалле льда I расположены в вердшнах тетраэдра. В 1957 г. Петерсон и Леви с помощью дифракции нейтронов показали, что атомы водорода обычно находятся на расстоянии - 1 0 А от одного из концов связи О-О и энергия их одинакова в любом положении. [7]
После того как У. Н. Брэгг [39] предложил расположение атомов кислорода во льду, показанное на рис 3.1, лед I, состоящий из молекул Н20 и ОЛЭ, широко изучали с помощью рентгенографии и методами дифракции электронов и нейтронов. Несомненно, что такое расположение атомов кислорода во льду I в основном корректно. Однако некоторые его детали остаются еще неопределенными. Принято, что единичная ячейка содержит четыре атома кислорода и имеет симметрию Рбз / ммк. Неопределенности структуры связаны с точностью определения размеров единичной ячейки и их зависимостью от температуры. [8]
Наиболее интересная особенность структуры заключается в расположении атомов кислорода относительно атома иридия. Оказалось, что атомы кислорода находятся на одинаковом расстоянии от иридия, а расстояние их друг от друга составляет 1 30 А. [9]
Йодная кислота имеет нормальную формулу HsIOe с октаэдри-ческим расположением атомов кислорода вокруг атома иода, как показано на рис. 8.2. Такое различие в составе этой молекулы и аналогичной молекулы хлорной кислоты НС1О4 обусловлено большими размерами атома иода, вокруг которого могут разместиться шесть атомов кислорода вместо четырех. [10]
В этом смысле термин структурная вода, означающий расположение атомов кислорода оксигидрильных групп в узлах решетки кристалла, является более определенным. Тем не менее даже и он отражает единственный геометрический признак оксигид-рильной группировки, упорядоченное расположение атомов кислорода, который существен скорее для всего кристалла в целом, но никак не характеризует строения самой ОтНп-группи-ровки. Не меняют положения и те уточнения понятия структурная вода, которые появились позже. [11]
 |
Положение целлобпознык цепей. [12] |
Они считают, что выбранные в этой модели направления цепей главных валентностей и расположения атомов кислорода недостаточно обоснованы. Кроме того, они оспаривают предположение о связывании ценой водородными мостиками. [13]
Таким образом, кристаллическая решетка имеет вакансии ( незанятые места) в узлах расположения атомов кислорода, а в кристаллической решетке TiOi oc избыточные атомы кислорода внедрены в междоузлия решетки. Благодаря наличию пустот или избыточных внедренных атомов в кристаллических решетках некоторые материалы проявляют много новых интересных свойств, например полупроводниковые. [14]
Таким образом, кристаллическая решетка TiOi имеет вакансии ( незанятые места) в узлах расположения атомов кислорода, а в кристаллической решетке TiOi j, избыточные атомы кислорода внедрены в междоузлия решетки. [15]
Страницы: 1 2 3 4