Расположение - молекула - вода
Cтраница 2
С одной стороны, ионы деформируют решетчатое расположение молекул воды. Этот эффект преобладает в случае анионов и зависит главным образом от размера ионов. Чем крупнее ионы, тем больше стерический деформационный эффект, и поэтому вызванные большими ионами деформация и разрыв водородных связей между молекулами воды простираются на большие расстояния. Повышение температуры также приводит к разрыву водородных связей, однако эти эффекты различного происхождения и мало похожи друг на друга. [16]
Образование водородных связей приводит к такому расположению молекул воды, при котором они соприкасаются друг с другом своими разноименными полюсами. Молекулы образуют слои, причем каждая из них связана с тремя молекулами, принадлежащими к тому же слою, и с одной - из соседнего слоя. [17]
Образование водородных связей приводит к такому расположению молекул воды, при котором они соприкасаются Рис 7 1 Ст к ДРУГ с Другом своими разноименными полюсами. [18]
Для сравнительной характеристики гидратации предложено использовать значение плотности расположения молекул воды в ближайшем окружении иона, не забывая, что в ближайшем окружении иона происходит постоянная смена молекул воды. [19]
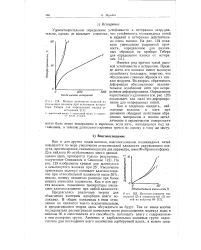 |
Влагопоглощение вытянутой ( 2 и невытянутой ( 1 нитей из найлона 66. [20] |
Тем не менее многие исследователи рассматривали возможное место расположения молекул воды в найлоне 66 и сопоставляли его способность поглощать влагу с содержанием-в нем полярных групп. [21]
Следовательно, аксиальная симметрия ЛМП является случайным следствием специфического расположения молекул воды в данной структуре. [22]
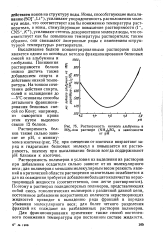 |
Растворимость яичного альбумина в. [23] |
Ионы, способствующие высали-ванию ( 5О5 - Ы), усиливают упорядоченность расположения молекул воды, что соответствует как бы понижению температуры растворителя, а ионы, стимулирующие повышение растворимости ( 1 -, CNS, К), усиливают степень дезориентации молекул воды, что соответствует как бы повышению температуры растворителя; таким образом, они связывают лиотропные ряды с изменением структурной температуры растворителя. [24]
Для цеолитов с более открыто структурой каркаса рентгеновские исследования указывают на отсутствие порядка в расположении молекул воды в каналах цеолитов. [25]
Метод основан на экспериментально установленной зависимости [47] коэффициента распределения экстрагируемой соли от величин поверхностной плотности расположения молекул воды в первой координационной сфере высаливателей и высаливаемой соли. [26]
Рассчитанные значения энергии наиболее информативны, если представлены в трех измерениях в форме карты с указанием расположения молекул воды, установленного кристаллографическим методом. [27]
 |
Изменение энтальпии плавления ( а и испарения ( б в ряду водородных соединений элементов VI группы. [28] |
Исследование процесса перехода молекул воды из жидкой фазы в газообразную также доказывает существование водородных связей и высокий порядок расположения молекул воды в структуре жидкостк. Истинная же температура кипения воды 100 С. С выше ожидаемой, что объясняется наличием в структуре воды водородных связей, препятствующих разрушению льдоподобной жидкой структуры. [29]
В самом приближенном виде моющее действие мыл можно объяснить следующим: на поверхности воды существует своеобразная пленка, возникающая благодаря специфическому расположению молекул воды у поверхности. При попадании мыла в воду происходит резкое снижение поверхностного натяжения вследствие того, что молекулы мыла, располагаясь а поверхности воды, нарушают прочную поверхностную пленку воды. Это происходит потому, что каждая молекула мыла состоит из длинной углеводородной цепи, имеющей гидрофобный характер ( отталкивается от воды), и группы гидрофильного характера ( притягивается к воде), например карбоксильной, причем взаимное притяжение между углеводородными частями молекул мыла значительно меньше, чем между молекулами воды. [30]
Страницы: 1 2 3 4