Расположение - уровни
Cтраница 2
Учитывая особенности в расположении уровней тяжелых и легких ядер, можно заключить, что у легких ядер интервал энергии, в котором действует закон 1 / т, будет гораздо больше, чем в случае тяжелых ядер. [16]
Для большого класса углеводородов расположение уровней, указанное на представленных выше диаграммах, является типичным. Все радикалы характеризуются наличием несвязывающей орбиты с WQ. В валентнонасыщенных углеводородах несвязывающие орбиты отсутствуют, а связывающие и разрыхляющие орбиты симметрично расположены относительно нуля отсчета энергии. [17]
Для большого класса углеводородов расположение уровней, указанное. Все радикалы характеризуются наличием несвязывающей орбиты с WQ, относительно которой симметрично располагаются уровни с отрицательными и положительными значениями W. В валентнонасыщенных углеводородах несвязывающие орбиты отсутствуют, а связывающие и разрыхляющие орбиты симметрично расположены относительно нуля отсчета энергии. [18]
Если Е 0, расположение уровней соответствует схеме для случая сильного поля. Напротив, при 0 преобладают корреляционные силы и основному состоянию соответствует максимальная мультиплетность. В табл. 2.12 приведены значения S, N и A. Очевидно, что в состоянии, которое соответствует сильному полю, скорее всего могут находиться ионы с шестью d - электронами, так как для этого состояния A. V равно всего 4, в то время как A. Действительно, опыт показывает, что ионы Со3, имеющие указанную конфигурацию, часто находятся в низкоспиновом состоянии ( S 0) даже в случае не слишком сильного поля, с которым мы имеем дело в окислах. В этих случаях усиливается тенденция к спариванию спинов за счет ковалентной связи и обусловленного этим ослабления корреляции. [19]
Что же касается порядка расположения уровней в Пределах данного мультиплета, то оказывается, что если число эквивалентных электронов в атоме или ионе меньше, чем половина от полного числа электронов, то в таком атоме мультиплеты Имеют нормальную структуру. В атомах и ионах, у которых число эквивалентных электронов больше ил равно половине от полного Числа электронов, мультиплеты будут обращенными. Например, У атома кислорода из восьми атомов четыре находятся в 2р - со-стоянии ( структура 2р4) и являются эквивалентными. Поэтому У атома кислорода мультиплеты являются обращенными. [20]
В случае обратного порядка расположения уровней излучает лиганд. [21]
Более полную информацию о расположении уровней и их устойчивости дают молекулярные орбитали. [22]
Такое же соответствие в расположении уровней энер гии имеется в ряду Li, Be, В2, С3, из чего следует заключить, что остов атома углерода, если не говорить о ядре, соответствует остову атома гелия. Сравнивая схемы уровней, приведенные на рис. 70 и 71, можно заключить, что у алюминия третий присоединяющийся к остову атома А13 электрон связан иначе, чем два электрона, присоединившиеся до него. Из правой половины рис. 71 видно, что у ионизированного углерода С валентный электрон находится в нормальном состоянии на 2 / - уровне. Электронное облако, символизирующее вероятность его нахождения вблизи ядра, имеет не симметрию шара, которой обладают электронные облака двух электронов, присоединяющихся после образования гелиевой оболочки, а только симметрию вращения. Четвертый внешний электрон, по спектральным данным, также находится на 2р - уровне. Таким образом, из четырех внешних электронов нейтрального атома С два находятся на 2 / - уровне и два - на 2х - уровне. Два последних электрона обладают антипараллельными спинами. Энергетические уровни внешних электронов, аналогичные уровням углерода, определяются из спектральных термов для кремния: два электрона на 3s - и два электрона на 3 -уров-не; это же справедливо и для других аналогов углерода, которые, следовательно, в противоположность элементам побочной подгруппы IV группы не только химически, но и спектроскопически аналогичны обоим наиболее легким элементам главной подгруппы. [23]
 |
Уровни энергии парамагнитного кристалла в функции магнитного поля. [24] |
При наличии внешнего магнитного поля расположение уровней зависит не только от напряженности магнитного поля, но и от взаимной ориентации внешнего магнитного поля относительно оси кристалла. [25]
Далее, отметим, что расположение уровней MI в верхней и нижней частях рисунка - обратное и, наконец, что переходы происходят только между уровнями с одинаковым значением MI. Эти выводы подтверждают ту интерпретацию спектра ЭПР атома водорода, которая дана в разд. [26]
На рис. 2.6 схематически представлено расположение уровней валентной зоны и зоны проводимости соответственно у металлов, полупроводников и изоляторов. [27]
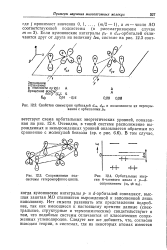 |
Свойства симметрии орбиталей dxi, dyz и возможности их перекрывания с орбиталями pz.| Сопряженные подсистемы гетероморфного цикла. [28] |
Очевидно, в такой системе расположение вырожденных и невырожденных уровней оказывается обратным по сравнению с молекулой бензола ( ср. [29]
Приведенная на рис. 2 схема расположения уровней имеет самый общий предварительный характер и требует дальнейших подтверждений. [30]
Страницы: 1 2 3 4