Большая величина - энергия - активация
Cтраница 1
Большая величина энергии активации ( 13 ккал / моль), катализируемой реакции с изопропиловым и mpem - бути-ловым спиртами весьма неожиданна. Очень сомнительно, чтобы катализируемая реакция с изопропиловым спиртом имела бы большую величину энергии активации, чем некатализируемая. [1]
Большая величина энергии активации также указывает на то, что частотный фактор в уравнении, определяющем скорость реакции, характеризующий процесс возврата, должен быть большим. [2]
Большая величина энергии активации ( 13 ккал / моль), катализируемой реакции с изопропиловым и mpem - бути-ловым спиртами весьма неожиданна. Очень сомнительно, чтобы катализируемая реакция с изопропиловым спиртом имела бы большую величину энергии активации, чем некатализируемая. [3]
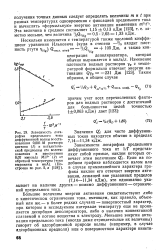 |
Зависимость логарифма предельного. тока диффузионной волны восстановления 0 001 М раствора цистина ( 1 и каталитиче. [4] |
Большие величины энергии активации свидетельствуют либо о кинетическом ограничении тока, имеющем, как правило, объемный или же - в более редких случаях - поверхностный характер, при котором в исследуемом интервале температур еще не проявляется десорбция деполяризатора, либо о наличии конвективной слагаемой в потоке вещества к электроду. [5]
Большие величины энергии активации свидетельствуют либо о кинетическом ограничении тока, имеющем, как правило, объемный или же. [7]
Большая величина энергии активации разветвления, чем окисления в конечные продукты, должна, однако, при повышении температуры привести к увеличению удельного веса разветвления. На деле же в температурном интервале, в котором наблюдается отрицательный температурный коэффициент, происходит обратное явление - разветвление становится все меньшим и можно думать, что в точке с нулевым значением температурного коэффициента разветвление практически полностью элиминируется. [8]
Большая величина энергии активации распада углеводородов также приводит к заключению, что реакции термич. [9]
Вследствие большой величины энергий активации двух разбираемых процессов их относительное значение резко изменяется с ростом температуры, и чем она выше, тем больше роль окиси этилена в образовании углекислого газа. [10]
Какие из указанных признаков: а) большая величина энергии активации; б) малая величина энергии активации; в) большой квантовый выход; г) малый квантовый выход; д) резкая зависимость скорости реакции от способа ее инициирования; е) уменьшение скорости реакции с течением времени; ж) увеличение скорости реакции с течением времени; з) малый температурный коэффициент скорости реакции; и) большой температурный коэффициент скорости реакции; к) экспериментальное обнаружение свободных атомов и свободных радикалов в реакционной смеси; л) малая чувствительность к присутствию посторонних примесей - свидетельствуют о цепном механизме реакции. [11]
Термическое разложение волокон полиакрилонитрила и поливинилового спирта характеризуется большими величинами энергии активации и предэкспоненциального множителя по сравнению с порошками. [12]
Исследование кинетики реакции разложения кумола на цеолите дифференциальным методом позволило обнаружить большую величину энергии активации и протекания на нем ( до 528 С) реакции крекинга кумола в кинетической области. Для реакции крекинга кумола на цеолите энергия активации равна 35 ккал. [13]
Здесь уместно ожидать, что скорость десорбции реагентов или продуктов велика, несмотря на большие величины энергий активации таких процессов. Однако в 1930 - 1940 гг. был изучен ряд реакций, легко протекающих при низких температурах. Из них особенно интересны обратимые реакции орто - и пара-превращения водорода и дейтероводородного обмена. Скорости этих реакций на переходных металлах типа вольфрама при - 80 очень близки и имеют один и тот же порядок, несмотря на разницу в энергиях активации. Бонхоффер и Фаркаш [5] предложили достаточно правдоподобный механизм, согласно которому водород адсорбируется в виде атомов с последующими конверсией или обменом после их десорбции. Однако опыты, проведенные Робертсом [6] по измерению величины и скорости адсорбции водорода на чистых вольфрамовых проволоках и скорости его десорбции, вызвали сомнения относительно этого механизма. Он показал, что даже при низких температурах водород действительно очень быстро адсорбируется в виде атомов с теплотой адсорбции, уменьшающейся от 40 ккал / моль при малых степенях заполнения поверхности приблизительно до 18 ккал / моль при почти полном насыщении поверхности. Однако при температурах до 400 десорбция протекает исключительно медленно. Эти соображения привели Ридила [7] к предположению, что данные реакции протекают между адсорбированными атомами ( удерживаемыми сильными связями) и молекулами, удерживаемыми на поверхности сравнительно слабыми силами Ван-дер - Ваальса и образующими физически адсорбированный, или вандерваальсов, слой. Обмен хемосорбированного атома с одним из атомов физически адсорбированной молекулы ( считалось, что такие молекулы располагаются в зазорах, имеющихся в хемосорбированном слое) должен быть почти термонейтральным и поэтому обладать малой энергией активации, делающей возможным протекание процесса обмена при низкой температуре. [14]
Хемосорбция происходит с большой скоростью даже при температуре жидкого воздуха, и необратима вследствие большой величины энергии активации десорбции. [15]
Страницы: 1 2 3 4