Распределение - метка
Cтраница 2
Применяемые для измерения Ег и Еа методы включают сравнение распределения метки в питающем растворе и вытекающей из исследуемой насадки жидкости при установившемся течении. Решения уравнения (4.47) при подходящих для используемого метода измерений граничных условиях сопоставляют с экспериментальными данными, чтобы найти значения коэффициентов перемешивания. [16]
Однако сначала следует отметить некоторые ранее не упомянутые детали, касающиеся распределения метки. Было найдено, что концентрация диоксиацетонфосфата значительно превышает концентрацию глицеральдегидфосфата. После очень кратковременных экспозиций в присутствии С1402 отношение С14: С12 для диоксиацетонфосфата имеет меньшую величину, чем для глицеральдегида, из которого он образовался. Следовательно, диоксиацетонфосфат характеризуется меньшей удельной активностью концевого углеродного атома, чем глицераль-дегидфосфат. [17]
Эти изящные опыты ясно показывают, что во всех изученных случаях распределение метки при редупликации ДНК находится в соответствии с предположением Уотсона и Крика; однако опыты не дают ответа на вопрос о том, вся ли двойная спираль ДНК раскручивается перед редупликацией. Действительно, такое раскручивание при рН и температуре, характерных для внутриклеточной среды, должно, по-видимому, происходить слишком медленно для обеспечения наблюдаемой скорости биосинтеза ДНК. Естественно поэтому предположить, что раскручивание двухцепочечной матрицы и спирализация новообразованных молекул ДНК происходят синхронно и поддерживаются ферментативными реакциями, ответственными за синтез полииуклеотидов. [18]
Другой проблемой, относящейся к мечению белков радиоактивным иодом, является степень гомогенности распределения метки в белке. В идеале желательно иметь материал, который постоянно содержит только 1 или 2 атома иода на молекулу белка, так как это соответствует наименьшим возможным изменениям протеина. [19]
Для модификации остатков тирозина в инсулине Де Зетен [31, 32] использовал I131, после чего определял распределение метки между 4 остатками тирозина. За исключением Туг А19, образующего монопроизводное, все указанные остатки присутствовали в виде ДИТ. [20]
Относительные скорости рассмотренных двух реакций для фенилциклопентана различаются незначительно, причем индукционный период до момента начала распределения метки между атомами углерода циклопентильнои группы также уменьшается. Таким образом, внутримолекулярные гидридные переносы прежде всего зависят от содержания катализатора, тогда как скорость переалкилирова-ния алкильных групп определяется температурой реакции. [21]
В контакт-ионной паре два атома кислорода карбоксилатного аниона валентны, и процесс внутреннего возврата приводит к ста-скому распределению метки 18О между обоими атомами юрода карбоксилат-иона. Однако для рацемизации требуется, бы анион и - О2М - С6Н4СОО - перешел с одной стороны бенз-ного катиона на другую его сторону. Очевидно, этот про-гораздо легче осуществляется в сольватно-разделенной, чем контактной ( тесной) ионной паре. [22]
Таким образом, данные Кристоля не согласуются, на первый взгляд, с данными Робертса [227] по распределению метки С14 при сольволизе того же брозилата в уксусной кислоте. Однако Ли [229] показал, что это противоречие является кажущимся и обусловлено различной температурой, при которой проводили эксперименты Роберте и Кристоль. [23]
В 1956 г. был поставлен специальный опыт, в котором эту РНК метили Р32 и после щелочного гидролиза изучали распределение метки в мононуклеотидах. [24]
На одной из стадий расщепления биосинтетического холестерина, полученного из меченого ацетата, Корнфорз, Хантер и Попжак [ 8 [ для установления распределения метки в кольце А превратили А5 - холестен в озон ид с 80 % - ным выходом, пропуская О. [25]
Они установили, что метка, первоначально находившаяся в одной фенильной группе, равномерно распределяется по всем трем группам со скоростью, равной скорости распределения метки на одном из этановых атомов углерода между обоими атомами этой группы, а также равной скорости обмена меченой ацетатной группы с ацетатными группами среды. Такая относительно высокая скорость перераспределения метки между фенильными группами не может быть объяснена с помощью предположения о промежуточном образовании циклогексадиенилия, который образуется при каждом переносе фенильной группы. Таким образом, при такой перегруппировке образуются два промежуточных иона карбония, в одном из которых заряд находится на конечном, а в другом - на начальном месте миграции; равновесие между этими ионами устанавливается быстрее, чем происходит их исчезновение путем захвата ацетатного иона. [26]
В: С: 0 12 5: 12 5: 1; / - межмолекулярный пере -, нос циклоалкильных групп; 2 - распределение метки С между атомами циклоал-кильной группы. [27]
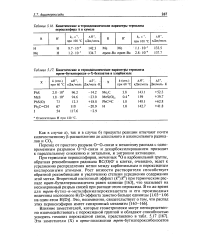 |
Кинетические и термодинамические параметры термолиза пероксиэфира А в кумоле.| Кинетические и термодинамические параметры термолиза mpew - бутилперокси-о - Х - бензоатов в хлорбензоле. [28] |
При термолизе пероксиэфиров, меченных 18О в карбонильной группе, обратная рекомбинация радикала RC ( O) O в клетке, очевидно, ведет к усреднению распределения метки между карбонильным и пероксидным кислородными атомами. Рост вязкости растворителя способствует обратной рекомбинации и увеличению степени усреднения содержания этой метки. Вторичный изотопный эффект ( А / Аг) при термическом распаде игре / и-бутилпероксиацетата равен единице [163], что указывает на несинхронный разрыв связей при распаде этого пероксида. [29]
Однако рациональный выбор режима работы ускорителя, размеров образца, двусторонее облучение мишени, модулирование пучка в процессе блучения позволяют при необходимости и в этом случае добиваться достаточно высокой степени равномерности распределения метки. [30]
Страницы: 1 2 3 4