Распределение - дейтерий
Cтраница 3
HD и D2, за исключением области высоких температур, вследствие влияния сравнительно больших изменений в весе ( поскольку Н заменен на D) на функции распределения молекул. Таким же образом, распределение дейтерия между углеводородом и водородом обычно несколько отличается от величины, которая ожидается, если исходить из вероятностного распределения. [31]
Квин и Моулер [1642] исследовали масс-спектры пяти дейтерированных стиролов. Рассматривая основные направления диссоциации, они установили, что распределение дейтерия в стироле является случайным, и высказали предположение, что имеет место перегруппировка молекулярного иона в цикло-октатетраеновую структуру. Эта гипотеза подтверждается большим сходством масс-спектров циклооктатетраена и стирола. [32]
Полное распределение может быть выражено в виде суммы двух вероятных распределений атомов Н и D. Выраженное таким образом содержание дейтерия обозначаем 8Д и 8В; распределение дейтерия, вычисленное для Л 0 87, 8Л 0 97, Зв0 50, приведено в последней строке табл. 1 и, как видно, находится в удовлетворительном согласии с найденным экспериментально. HD в дейтерий, поскольку это отношение представляет собой резко меняющуюся функцию от S А, когда 8Л велико. [33]
Для проверки этой точки зрения были проведены опыты с н - и цзо-про-пилхлоридами, из которых соответственно должны образовываться адсорбированные н-пропильный и изо-пропильный радикалы. Эти соединения были медленно восстановлены дейтерием при 100, в результате чего получено распределение дейтерия ( см. табл. 3), подтверждающее неразличимость адсорбированных пропильных радикалов. [34]
Интересно отметить, что при разложении HGOOD на обычном формиате образовавшийся водород содержит только HD; ни Н2, ни Dig не образуются. Содержание дейтерия в OD-группах в HCOOD составляло около 85 %, и из распределения дейтерия в образовавшемся водороде ясно видно, что при разложении HCOOD на ( HCOO) Zn выделяется только HD, если принимать во внимание чистоту исходной HCOOD. При этих температурах обменная реакция между D2 и Н, на катализаторе была незначительна. [35]
Одним из методов получения информации об иптермедиатах каталитического гидрирования является исследование направления введения дейтерия, когда насыщенный углеводород распределяют на поверхности катализатора, насыщенной дейтерием. Ниже приведены пе-рвовйчзлыше продукте некоторых таких реакций частичного обмена, ( Длительная выдержка обычно приводят к более беспорядочному распределению дейтерия. [36]
Возникает вопрос, обладают ли бензильные анионы двойственным характером по отношению к донорам протонов. Для того чтобы выяснить это, Рассел [10] обрабатывал 2-фенил - 2-пропил-калий различными дейтеросодержащими кислотами и изучал распределение дейтерия в молекуле образующегося кумола. Дейтерирование в пара-положение происходит в большей степени, чем в ортоо-положение. Хотя хорошо было бы иметь такие же сведения и для других подобных систем, но и из имеющихся данных уже можно сделать вывод, что карбанион реагирует преимущественно таким образом, что восстанавливается ароматический характер системы. [37]
На D имеет ту же скорость и дает те же продукты, как с D2 Н2 Н, так что присутствие атомного D не влияет на обмен. Все эти данные приводят к выводу, что гомогенный обмен свободных радикалов в газовой фазе происходит непосредственно с молекулярным D2, причем из распределения дейтерия в продуктах обмена с радикалами видно, что в обмене участвуют лишь те атомы водорода, которые связаны с углеродом, непосредственно примыкающим к атому углерода, несущему радикальный электрон. Например, радикал этила CHR - CH2 с D2 дает лишь CH3CHD и CH3CD2, но в радикале метила СНз могут заместиться все три атома водорода. Отсутствие обмена в трифенилметиле в свете этих данных объясняется тем, что в этом радикале нет ни одного атома водорода, который удовлетворял бы указанному условию соседства с углеродом, несущим непарный электрон. Участие других атомов водорода в обмене, например, в циклогексане, объясняется изомеризацией радикала с перенесением свободного непарного электрона на другие атомы углерода. [38]
Результаты этого исследования не исключают, однако, возможности расщепления аллилфенилового эфира не на ионы, а на радикалы, так как в этом случае фенол-3 5 - с12 мог бы не быть акцептором образующихся аллильных радикалов. С целью исключения этого, вообще говоря, мало вероятного механизма и для дальнейшего проникновения в механизм реакции Клайзена, Фоменко и Садовникова [200] исследовали распределение дейтерия в продуктах совместной перегруппировки смеси цин-намилфенилового эфира ( е) и аллилфенилового-3 5 2 эфира ( ж) в ци-этиламиновом растворе. Выделенный из смеси о - ( а-фенилаллил) - фенол не содержал дейтерия, связанного с углеродом. [39]
Анализ данных Туркевича с соавторами [17] показывает, что при гидрировании этилена на никеле при 90 такие соотношения примерно выполняются. При более низких температурах общее количество обмененных этиленов уменьшается ( см. выше), но все они образуются уже не по последовательному механизму, а, по-видимому, по параллельным путям, - на всем протяжении процесса распределение дейтерия в них соответствует равновесному. В случае палладия такое изменение механизма обмена может быть связано с тем, что при 135 в Pd растворено значительно больше водорода, чем при 185 [25], и что, следовательно, концентрация адсорбированных на поверхности атомов должна быть значительно выше. Поэтому при 135 основным путем регенерации этилена может стать ассоциативный механизм. [40]
Нижний ряд значений отвечает скоростям обмена R на окислах ( 10 - 8 молъ / м х Хлшк) при 25 С, рассчитанным по уравнению N In ( 1 - х) Rt, где N - общее число молей этилена в реакторе. Окисел Со804 обладал исключительно высокой активностью, и равновесное превращение на нем достигалось за 5 мин даже при - 10 С. Распределения дейтерия в продуктах реакции на Со304, полученных при О С и - 10 С, согласуются со статистическими. [41]
В диметилсульфоксиде ( растворитель с высокой диэлектрической проницаемостью) промежуточным продуктом является, по-видимому, свободный карбанион. В нем все семь центров водородной связи становятся эквивалентными, и поэтому преобладающим процессом будет межмолекулярное протонирование. Хаотический характер распределения дейтерия в продукте, получаемом в триэтилкарбиноле, свидетельствует о том, что ион калия и связанный с ним дейтеросодержащий лиганд перемещаются вдоль цикла быстрее, чем происходит протонирование карбаниона. [42]
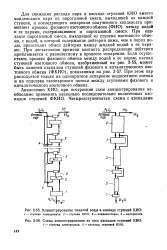 |
Концентрирование тяжелой воды в каскаде ступеней КИО.| Схема концентрирования из трех каскадов ступеней КИО. [43] |
Для снижения расхода пара в каскаде ступеней КИО вместо конденсации пара из парогазовой смеси, выходящей из каждой ступени, и последующего испарения полученного конденсата применяют процесс фазового изотопного обмена ( ФИО) между водой и ее парами, содержащимися в парогазовой смеси. При контакте парогазовой смеси, выходящей из ступени изотопного обмена, с водой, в которой содержание дейтерия ниже, чем в парах воды, происходит обмен дейтерия между жидкой водой и ее парами. При достаточном времени контакта распределение дейтерия приближается к равновесному в процессе испарения. При этом пар расходуется только на однократное испарение жидкостного потока и на подогрев газопарового потока между ступенями фазового и каталитического изотопного обмена. [44]
Было изучено влияние варьирования исходного соотношения дейтерий: циклопропан при 50 на распределение дейтерия в продуктах реакции. Оказалось, что это распределение не зависит от исходного соотношения. Как видно из таблицы, распределение дейтерия не зависит также и от температуры; минимум, отвечающий пропану-с / е, делит его на две части. [45]
Страницы: 1 2 3 4