Равновесное распределение - вещество
Cтраница 1
Равновесное распределение вещества между разделяемой смесью и растворителем или между двумя несмешивающимися фазами определяется законом распределения. [1]
Равновесное распределение вещества между фазами происходит в сосуде с фиксированным объемом ( рис. 2.11), газовое пространство которого соединяется с пробиркой для накопления вещества и медицинским шприцем на 50 мл. Когда объем сконденсированного газа достигает 50 мл ( поршень шприца опущен вниз до отказа), пробирку извлекают из жидкого азота, и сконденсированный газ начинает испаряться. Давление в системе возрастает, и поршень шприца начинает подниматься. Операция конденсации и испарения может повторяться многократно. По окончании накопления вещества пробирка, содержащая концентрат, с помощью специального устройства подключается к газовой схеме хроматографа, и при повышенной температуре потоком газа-носителя уловленные вещества переносятся в хроматографическую колонку. Следует, однако, отметить, что этот оригинальный способ применим в основном для качественных определений. Количественный анализ, особенно при многократных конденсациях, провести довольно сложно. [2]
Равновесное распределение вещества между рафинатом и экстрактом определяется законом распределения. [3]
Равновесное распределение вещества в объеме, как и всякое равновесие, не зависит от пути, каким оно было достигнуто. Примененный способ расчета этого распределения заключается в приравнивании диффузионного потока седнментационному и является только одним из возможных методов расчета. Более того, наличие переноса вещества в этом случае не является необходимым условием, поскольку в полученных формулах не содержится величина В, характеризующая перенос и связанное с ним трение. Равновесное распределение, найденное термодинамическим путем, может быть вычислено без учета механизма, по которому оно устанавливается. [4]
Равновесное распределение вещества между двумя сосуществующими фазами определяется взаимодействием молекул растворенного вещества с молекулами растворителей или, точнее, потенциальными энергиями молекул растворенного вещества в поле молекул растворителей. [5]
 |
А. Схема дозирования в хроматограф равновесного пара по Пуш-ману [ 3. [6] |
Для установления равновесного распределения вещества в статических условиях благодаря простоте, доступности и невысокой стоимости широко используются сосуды с постоянным объемом. В качестве таких емкостей обычно применяется стандартная лабораторная посуда, но чаще всего стеклянные флаконы с внутренним объемом 5 - 40 мл, закрывающиеся эластичной резиновой пробкой. Отбор проб равновесного газа из сосуда и дозирование его в испаритель хроматографа производится медицинскими или специальными газовыми шприцами. [7]
Развитие взглядов на природу равновесного распределения вещества связано с развитием представлений о природе неидеальности растворов. Современные представления теории распределения близка соприкасаются с теорией неидеальности Ван-Лаара и Гейтлера. [8]
Массооб-менные процессы основаны на неодинаковом равновесном распределении веществ между двумя взаимнонерастворимыми фазами. В случае жидкостной экстракции обе фазы, между которыми происходит массо-обмен, являются жидкими. [9]
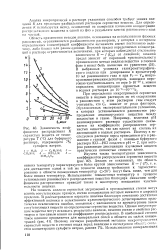 |
Зависимость коэффициента распределения К сернистых веществ от температуры Т ( СС для буферного раствора, содержащего 7 % сульфата натрия. [10] |
Использование повышенных температур в процессе установления равновесного распределения вещества благодаря снижению коэффициента распределения приводит также к некоторому повышению чувствительности анализа. [11]
Допустимую скорость элюции определяют процессы установления равновесного распределения вещества между подвижной и неподвижной фазами. Подробно эти вопросы были рассмотрены в гл. Было показано, что равновесие устанавливается тем быстрее, чем меньше размеры гранул и крупнее поры. Для больших молекул биополимеров с их замедленной диффузией время установления равновесия в хроматографических зонах увеличивается весьма существенно, так что скорость элюции должна быть соответственно уменьшена. [12]
V и выдержи-вают при постоянной температуре до установления равновесного распределения вещества между жидкой и газовой фазами. [13]
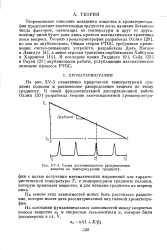 |
Схема установившегося распределения веществ по температурному градиенту. [14] |
На рис. XV-3 схематично представлен температурный градиент колонки и равновесное распределение веществ по этому градиенту. [15]
Страницы: 1 2 3 4